ALSという病気を知っているだろうか?
『ALS…筋萎縮性側索硬化症(きんいしゅくせいそくさくこうかしょう、英語:amyotrophic lateral sclerosis、略称:ALS)は、重篤な筋肉の萎縮と筋力低下をきたす神経変性疾患で、運動ニューロン病の一種。極めて進行が速く、半数ほどが発症後3年から5年で呼吸筋麻痺により死亡する(人工呼吸器の装着による延命は可能)。治癒のための有効な治療法は現在確立されていない。
ウィキペディアより』
広告プランナーの藤田正裕さん(通称ヒロさん)は、
30歳を目前にALSを発症した。
ヒロさんのご著書
『99%ありがとう ALSにも奪えないもの』
を読んだときの衝撃は忘れられない。
その一部を紹介させていただく。
------------------------------------------
■常に死にたいと思う、そして生きたいとも思う。
その繰り返し。
それが闘い。
恐怖。
いっぱい話すと、疲れて、
舌と口が思うように動かなくなってきた。
徐々に顔に来てる…。
声を取られて3か月で、もう口パクもか。
どうやって戦えばいいかわかんない相手、どう倒せばいいんだ。
チクショー。
目しか動かなる恐怖。
目も動かなくなる恐怖。
今朝も目が覚め、その先の状態を考えてしまい、パニック。
自殺の思いに襲われ続けながら、自分を落ち着かせた。
希望と絶望ってホントに隣合せ。
■ 一秒も休んでない。
人に一番伝えにくい、わかってもらいにくいことは、
「毎秒」闘っているということ。
休憩とか、リフレッシュとか、一服とか、「ほっ」とする瞬間がほぼない。
映画を見たりとか、安定剤を飲んでどうにか現実逃避がてきても「ほっ」とは3年間してない。
毎日神経が張っている。
毎秒。
それを僕よりはるかに長い時間、家族、友達もいないまま、
10年、20年と耐えている方たちもいる。
そのうえ、目も動かなくなった方々もいる。
毎秒、狂わないように脳の中でなにを行っているのだろうか。
ゲーム?思い出を振り返ってる?
想像できない。
一秒でも早く解放を…。
------------------------------------------
ヒロさんは、いろんな人から
「強いですね!」
と言われるそうだ。
でも、彼は
「俺は決して強くない。
なんどもなんども戦いに挑んでは負けている」
と言っている。
ヒロさんが出演していたテレビ番組で、
「生きるとはなんだと思うか?」と質問されたときの答え…
「生きるとは、楽しむことだ。」
私も、もがき苦しんでいるときに、この言葉を何度も何度も心の中で唱える。
「生きるとは、楽しむことだ!」
「生きるとは、楽しむことだ!」
「生きるとは、楽しむことだ!」
今をもがき苦しんでいる人へ。
どうか人生を楽しむことを忘れないでほしい。
ヒロさんのホームページは、ココ。
どうかALSをまず知ってほしいです。
一秒でも長くほっとできる時間、心安らかなときが訪れることを祈って。
苦しんでいる人へ。
大好評!『壁orノートに貼って覚える化学 ポイント・まとめ集』
『壁orノートに貼って覚える化学ポイント・まとめ集』の無機化学編と有機化学編をご購入されたお客様から「もっと早く欲しかった!」との声が続々届いていますので、
ここでまた紹介させていただきます。
pdfデータなので、プリントアウトし放題!
トイレや自分の部屋の壁に貼ったり
ノートに貼ったり
目につくところに貼りまくって
覚えてください!
このまとめ集はとにかく試験にでるところがつまっています!
■特徴1
全国の国公立私大の入試問題(過去7年分)が入力されたデータベースソフトを用いて,徹底的に入試に出るポイントを分析。
■特徴2
他の参考書には載っていない,見たことのないようなポイントやまとめ表を掲載。
例えば……
□X線の遮蔽剤といえば?
X線の造影剤と言えば?
マニアックな知識ではなく,これらは意外と入試で出題されています!
こんな形で掲載
↓ ↓ ↓ ↓
□硫化カドミウムCdS,クロム酸鉛(Ⅱ)PbCrO4,酸化亜鉛ZnO,硫酸バリウムBaSO4,酸化鉄(Ⅲ)Fe2O3
これらに共通する用途は?
こんな形で掲載
↓ ↓ ↓ ↓
□ケイ素Si,リンP,硫黄Sの単体にうち天然に存在するものは?
こんな形で掲載
↓ ↓ ↓ ↓
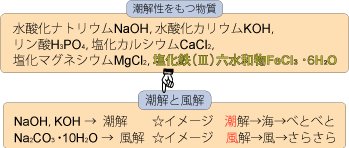
□水酸化ナトリウムNaOH,水酸化カリウムKOH,リン酸H3PO4,塩化カルシウムCaCl2,塩化マグネシウムMgCl2,塩化鉄(Ⅲ)六水和物
これらの物質に共通する性質は?
こんな形で掲載
↓ ↓ ↓ ↓
□6つの主要なアセトンの製法を言えますか?
こんな形で掲載
↓ ↓ ↓ ↓
□2つの主要な乾留の反応を言えますか?
こんな形で掲載
↓ ↓ ↓ ↓
■特徴3
くらべてつなげてまとめる表を多数掲載
人間の脳は、事柄と事柄をシナプスで繋ぎ、記憶していくことから、英単語などを記憶する際には、グループごとに分類したり、関連するイメージでつなげて覚えていくと、効率的に語彙を増やし、忘れにくいことなどが知られています。
そこで,くらべてつなげて覚えられるようにまとめました。
例えば……
こんな形で掲載
↓ ↓ ↓ ↓
■特徴4
豊富な色を使用。
化学は,呈色反応や化合物などの色を問う問題がよく出題されることから,色がついた文字色を何度も見ることによって記憶がより定着します。
例えば……
□白煙が生じる2つの反応を挙げられますか?
こんな形で掲載
↓ ↓ ↓ ↓
□銅と銀の主要な化合物の色を言えますか?
こんな形で掲載
↓ ↓ ↓ ↓
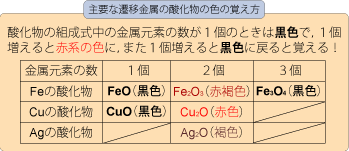
□典型・遷移金属の主要な酸化物の色を言えますか?
こんな形で掲載
↓ ↓ ↓ ↓
□主要な水和物の色を言えますか?
こんな形で掲載
↓ ↓ ↓ ↓
■特徴5
「キーワード連想」を掲載
当然ながら、入試は時間が勝負です。
そこで,あるキーワードがでたら,ポイントがすぐに連想できるようになるようにまとめました。
例えば…
□天然ガスから分離 or 沸点が最も低い or イオン化エネルギーが最も大きい or 最も理想気体に近い気体とあったら?
□空気中で最も多く存在する希ガスとあったら?
□白色顔料,医薬品,化粧品とあったら?
□黒い多量のススとあったら?
□果実の成熟作用,植物ホルモンとあったら?
□強い光を放って燃焼とあったら?
こんな形で掲載
↓ ↓ ↓ ↓
★他にも掲載している例を紹介します。
□リン酸カルシウムからリン酸までの反応の流れが言えますか?
こんな形で掲載
↓ ↓ ↓ ↓
□二酸化ケイ素からシリカゲルまでの反応の流れが言えますか?
こんな形で掲載
↓ ↓ ↓ ↓
□次の酸のうち揮発性の酸はどれですか?
硝酸,塩酸,フッ化水素酸, 酢酸,濃硫酸
こんな形で掲載
↓ ↓ ↓ ↓
□希硫酸と濃硫酸の性質を言えますか?
こんな形で掲載
↓ ↓ ↓ ↓
□無機化学において,水素が発生する頻出の反応を何個挙げられますか?
こんな形で掲載
↓ ↓ ↓ ↓
□次のアルミニウムに関する用語を説明できますか?
ボーキサイト,アルマイト,アルミナ,ジュラルミン,テルミット
こんな形で掲載
↓ ↓ ↓ ↓
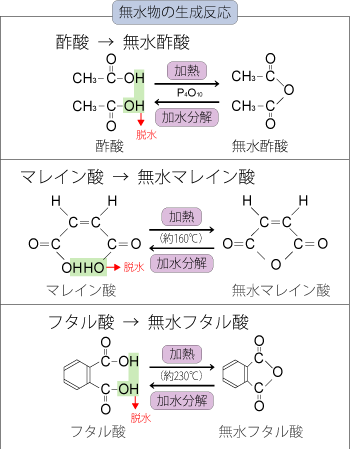
□混同しやすい無水物の生成反応
こんな形で掲載
↓ ↓ ↓ ↓
□有機化合物のにおい
こんな形で掲載
↓ ↓ ↓ ↓
□ナトリウムフェノキシドの2つの生成反応
こんな形で掲載
↓ ↓ ↓ ↓
□有機化合物で登場する水酸化ナトリウムNaOHの反応
こんな形で掲載
↓ ↓ ↓ ↓
□混同しやすい有機化合物の反応
こんな形で掲載
↓ ↓ ↓ ↓
□こんな図表とか
↓ ↓ ↓ ↓
これらはほんの一部です!
この『壁orノートに貼って覚えるポイント・まとめ集』を壁やノートに貼って毎日眺めることで暗記が大幅に短縮できます!
pdfデータ形式になっているので,何枚でもプリントでき,いろんなところに貼ったり,携帯することができます。
絶対にお得です!
下記は,有機化学編の表紙(A4サイズ)です。
下記,DLマーケットよりご購入いただけます。
【壁orノートに貼って覚えるポイント・まとめ集 有機化学編】
pdfデータ(A4サイズ 12枚) 価格 1,000円
【壁orノートに貼って覚えるポイント・まとめ集 無機化学編】
pdfデータ(A4サイズ 17枚) 価格 1,000円
「浸透圧に関する問題 完全攻略チャート&過去問解説集」販売のお知らせ
分子やイオンの粒子の大きさは、物質によって異なります。したがって、ある大きさ以上の粒子を通さない穴の空いた膜を用いれば、その大きさによって物質を分けることができます。
このような膜を半透膜とよびます。
図1のようにU字管を準備し、溶媒分子を通し、溶質粒子は通さない半透膜を中央部分に取り付け、左側に溶液、右側に溶媒を両液面の高さが等しくなるように入れ、長時間放置します。
すると、溶媒分子は溶媒側から溶液側に向かって半透膜を通って移動(浸透という)し、両液面差が一定となったところで溶媒分子の移動が止まります。(図2の状態)
このとき溶液の液面を、もとの高さにするために必要な圧力を浸透圧(図3 紫色の矢印)といいます。
また、浸透圧は、溶媒分子が半透膜を通して溶液側に浸透しようとする圧力(橙色の矢印)であるともいえます。
浸透圧の計算問題は、ファントホッフの公式に数値をあてはめれば簡単!と思っている人が多いですが、中堅以上の大学の入試問題となるとそうはいきません。
特に、「U字管の液面差の絡む浸透圧問題」が圧倒的に多く出題され、その解答率は極端に低くなります。
その原因は、溶液柱の圧力をPaの単位に換算することがわからないためです。
また、浸透圧は希薄溶液の場合には、溶質の種類によらず、溶液のモル濃度C(mol/L)に比例します。
これより、比例定数を用いて次のように表されます。
Π=CRT
このときの溶液のモル濃度C(mol/L)は、溶液中での溶質の物質量で、例えば、電解質は水溶液中で電離するため、同濃度の非電解質の水溶液に比べて溶質の粒子(イオンや分子)数が多くなります。
したがって、溶質の物質量は粒子の総物質量で考えなければいけないません!
浸透圧の問題での総物質量の算出方法は、主に以下のⅠ~Ⅴの3タイプを覚えればよいでしょう。
Ⅰ.溶質が電離も会合もしないタイプ
Ⅱ.溶質が完全に電離するタイプ
Ⅲ.溶質が電離度αで電離するタイプ
完全攻略チャートでは、上記などを詳しくわかりやすくまとめています!
過去問解説集(問題のみはココでみれます)には、下記の大学が収録されています。
東京医科歯科大学(2013年)、広島大学(2013年)、横浜国立大学(2012年)、名古屋市立大学(2012年)、福井大学(2012年)、大阪市立大学(2012年)、東京理科大学(2010年)、中央大学(2010年)、千葉大学(2010年)、埼玉大学(2009年)
これらを圧倒的にわかりやすくまとめています。
これ以上わかりやすく丁寧に解説したチャート&過去問題解説集は他にはどこにもないでしょう!
商品(完全攻略チャート16枚 過去問解説集28枚 A4普通紙 全44枚)はHP「恋する化学」からご購入いただけます。
拙著
『くらべてつなげてまとめる数学 (数学Ⅰ、A、Ⅱ、Bをネットワークでつなぐ)/文英堂』
¥1、296
Amazon.co.jp
も宜しくお願い致します。
無機化学と有機化学の参考書は、下記DLマーケットにて販売しています。
【「くらべてつなげてまとめる無機化学」 第一部】
【「くらべてつなげてまとめる無機化学」 第二部】
【「くらべてつなげてまとめる有機化学」 第一部】
【「くらべてつなげてまとめる有機化学」 第二部】
↓ランキングが見れます。↓
にほんブログ村
↓ランキングが見れます。↓
にほんブログ村
典型元素と遷移元素に関する問題
2011年~2013年までで、典型元素と遷移元素に関して出題された全国の入試問題を徹底的に分析し,まとめてみました。
遷移元素に関する出題が圧倒的に多く,次の7つをおさえれば,ほぼ100%大丈夫でしょう。
特に,①,②,③,⑦が頻出です!
■遷移元素
①周期表の第4周期以降の3~11族に位置している。
②すべて金属元素である。
③最外殻電子は1個または2個で,ほぼ一定。原子番号が変わっても価電子の数がほとんどの元素で1個または2個であることから,となりあう元素の化学的性質も似ている。
④イオンや化合物には,有色のものが多い。
⑤単体や化合物は,触媒として用いられるものが多い。
⑥酸化数は,通常安定な+2あるいは+3のほかに,Mnに代表されるように多くの酸化数を示す。
⑦典型元素の金属の単体と比べて,融点や沸点が高く,密度の大きいものが多い。
■典型元素
①典型元素は,金属元素と非金属元素がある。
②周期表の1,2,12~18族に位置している。
下記は実際に出題された入試問題です。
上記のポイントをしっかり頭に入れたうえで挑戦してみましょう!
-------------------------------------------------
■2013年 大学入試センター 本試験 化学Ⅰ
問 元素の周期表に関する記述として誤りを含むものを,次の①~⑤のうちから一つ選べ。
① 2族元素の原子は,2価の陽イオンになりやすい。
② 17族元素の原子の価電子の数は,7である。
③ 18族元素は,反応性に乏しい。
④ 典型元素は,すべて非金属元素である。
⑤ 遷移元素は,すべて金属元素である。
□答え……④
※典型元素には,金属元素と非金属元素があります。
■2013年 京都産業大学 理 コンピュータ理工 総合生命科
遷移元素は,周期表第4周期以降の (1) 族~ (2) 族に位置する元素である。この元素は,熱や電気を導きやすい金属元素の一種で,たたくと薄く広がる性質( (3) 性)や引っ張ると細長く伸びる性質( (4) 性)がある。遷移元素の (A) 電子の数は1または2であり,それ以外の元素(典型元素)と異なり,同族元素だけでなく同一周期の隣り合う元素同士の性質が良く似ている。
問1 空欄(1)~(2)に適切な数値,空欄(3)(4)に適切な語句を記せ。
問2 空欄(A))に,以下の語群から適切な語句を選び,ア~ウの記号を記せ。
(A)〔ア:電子殻イ:内 殻ウ:最外殻〕
□答え……
問1
(1) ……3
(2) ……11
(3) ……展性
(4) ……延性
問2
(A) ……ウ:最外殻
■2013年 神戸学院大学 総合リハビリテーション 栄養
遷移元素に関する次の記述A~Fのうちから,誤っているものを1つ選べ。
A 周期表3~11族に属する元素を遷移元素という。
B すべて金属元素である。
C 単体は,典型元素の単体と比較して密度の大きいものが多い。
D 最外殻電子は3個または4個で,ほぼ一定である。
E イオンや化合物には,有色のものが多い。
F 単体や化合物は,触媒として用いられるものが多い。
□答え……D 最外殻電子は3個または4個で,ほぼ一定である。
※遷移元素の最外殻電子は1個または2個で,ほぼ一定です。
■2011年 中京大学 情報理工
問 元素の周期表に関する次の記述について,空欄 ア ~ オ にあてはまる最も適切な語句を,以下の解答群からそれぞれ1つずつ選べ。
周期表の同じ縦の列に並んだ元素は, ア と呼ばれる。 ア の中には,原子の イ 数が同じで性質が互いに良く似ているため固有の名称でよばれるものがある。例えば水素を除く1列目の ア は, ウ と呼ばれ,イオン化傾向が大きく, イ を放って1価の陽イオンになりやすい。このような周期表の縦の列に並んだ元素同士の性質が似ている元素は,1列目の他に,周期表の2列目および12~18列目に見られ,これらは エ と呼ばれている。一方で,3~11列目の元素は オ と呼ばれ,周期表の横の行に並んだ元素の性質が,似ていることが多い。
解答群
① アルカリ金属元素② アルカリ土類金属元素
③ 価電子④ 希ガス元素⑤ 原子番号⑥ 遷移元素
⑦ 中性子⑧ 典型元素⑨ 同族元素⑩ ハロゲン元素
⑪ 非金属元素⑫ 陽子
□答え……
ア……⑨ 同族元素
イ……③ 価電子
ウ……① アルカリ金属元素
エ……⑧ 典型元素
オ……⑥ 遷移元素
■2011年 東京慈恵会医科大学 医
A~Dに当てはまる数字または語句を答えよ。
周期表の第 A 族から第 B 族までの元素を遷移元素と呼び,第 C 周期元素では21Sc以降の元素が含まれる。以前には,30Znもこれに含める考え方があったが,現在は典型元素に分類されている。これは,遷移元素が,通常安定な+2あるいは+3の酸化数のほかに,25Mnに代表されるように多くの酸化数を示すのに対し,Znの同族元素には,最高+2の酸化数が知られるのみであるからである。この理由は,Zn2+イオンでは D 殻以下の電子殻がすべて閉殻となる電子配置をとることによる。一方,Mnには+2から+7までの原子価が知られている。酸化数の大きい酸化マンガン(Ⅳ)や過マンガン酸カリウム(KMnO4)は酸化剤として重要である。
□答え……
A 3
B 11
C 4
D M
■2011年 東京理科大学 B方式 薬
周期表と元素に関する次の設問に答えなさい。
(1)の文章中の空欄 (ア) ~ (エ) に最も適当な語句または記号を指定された解答群から選び,その番号を解答用マークシートの指定された欄にマークしなさい。また, ① ~ ④ には最も適当な数字を解答用マークシートの指定された欄にマークしなさい。
(1) 周期表の横の行を周期といい,第1周期から第7周期まである。周期表の縦の列を族といい,第1族から第18族まである。各周期の1, ① および ② ~18の各族の元素を (ア) ,また各周期の3~ ③ の各族の元素を (イ) とよぶ。(イ)は原子番号が変わっても (ウ) の数がほとんどの元素で1個または ④ 個であることから,となりあう元素の (エ) も似ている。
解答群Ⅰ 〔(ア)~(コ)の解答群〕
00 右 上01 右 下02 左 上03 左 下
04 弱 く05 強 く06 失 う07 得 る
08 典型元素09 遷移元素10 原子価11 価電子
12 軌道電子13 化学的性質14 物理的性質
□答え……
①……2
②……12
③……11
④……2
ア……08 典型元素
イ……09 遷移元素
ウ……11 価電子
エ……13 化学的性質
■2011年 東京理科大学 B方式 理2部
周期律や元素などの性質に関する以下の文章の (1) ~ (2 に,最も適切な語句をそれぞれの解答群から選び,その番号を解答用マークシートの指定された欄にマークしなさい。
周期表の中央部分に位置する3~11族の元素を (1) という。 (1) の価電子数は原子番号順に1個ずつ増加するが,第4周期では内側の電子殻で電子が増加していき,最外殻電子数は1個から最大で (2) 個までとりうる。 (1) は一般に酸化数やイオンの色が変化しやすい性質がある。
(1)の解答群
1 遷移元素 2 典型元素 3 非金属元素 4 アルカリ金属 5 アルカリ土類金属
(2)の解答群
1 1
2 2
3 3
4 4
5 5
□答え……
(1) 1
(2) 2
■2011年 同志社大学 生命医科 理工 スポーツ健康科 心理 文化情報
周期表で( あ )族から( い )族の元素は遷移元素とよばれ,日常生活で重要なものが多い。遷移元素の最外殻電子の数は( う )または( え )個であり,同一の遷移元素でも複数の酸化数を示すことが多い。
(1) 文中の空欄( あ )~( え )に最も適する数値を答えよ。
(2) 次の(ア)~(エ)の遷移元素に関する記述のうち,正しいものには「○」を,誤っているものには「×」を記入せよ。
(ア) 遷移元素の単体はすべて金属である。
(イ) 典型元素の金属の単体と比べて,遷移元素の単体は密度が大きいが,融点が低いものが多い。
(ウ) 遷移元素は典型元素と異なり,同族元素だけでなく同一周期の隣り合う元素とも性質がよく似ているものが多い。
(エ) 銅,銀,金は希硫酸には溶けないが,硝酸には溶ける。
□答え……
(1)
あ 3
い 11
う,え 2,1 (順不同)
(2)
(ア) ○
(イ) ×
※(イ) 典型元素の金属の単体と比べて,遷移元素の単体は密度が大きいが,融点が高いものが多いです。
(ウ) ○
(エ) ×
■2012年 星薬科大学 B方式 薬
問 次の記述のうち,正しいものを1つ選べ。
1.元素の周期表の10族から18族を典型元素という。
2.2族元素をアルカリ土類金属という。
3.元素の約20%は金属元素である。
4.遷移元素は,異なる族の元素でもよく似た性質を示すことが多い。
5.1族元素をアルカリ金属という。
□答え
……4
※元素の周期表の1,2,12族から18族を典型元素といいます。
※元素の約80%が金属元素です。
※水素Hをのぞく1族元素をアルカリ金属といいます。
※ベリリウムBeとマグネシウムMgを除く2族元素をアルカリ土類金属といいます。
ひっかけ問題でよく出題されるので注意しましょう!
■2012年 龍谷大学 A日程 理工
(1) 金属の結晶では,金属元素の原子が規則正しく並んで多数結合している。金属の結晶内では,原子から価電子が離れることができる。この価電子は,金属内を自由に動きまわり,〔 1 〕。この電子を自由電子という。このように金属には,自由電子があるため,〔 2 〕が大きい。周期表によれば,元素の約 が金属元素であることがわかる。元素は典型元素と遷移元素に分けられるが,典型元素の約半数が金属元素であり,遷移元素は〔 3 〕である。遷移元素は,周期表の第〔 4 〕周期以降の3~11族に位置している。
問1 空所〔 1 〕に当てはまる最も適当なものを,次の中から一つ選びなさい。解答番号 11
① イオン結合でつながっている
② 共有結合でつながっている
③ クーロン力によりつながっている
④ 結晶中の約半分の原子に共有されている
⑤ 結晶中のすべての原子に共有されている
⑥ ファンデルワールス力によりつながっている
問2 空所〔 2 〕に当てはまる最も適当なものを,次の中から一つ選びなさい。
① 吸湿性 ② 伸縮性 ③ 断熱性 ④ 電気伝導性 ⑤ 熱硬化性
問3 空所〔 3 〕に当てはまる最も適当なものを,次の中から一つ選びなさい。
① すべて金属元素
② すべて非金属元素
③ 約1/2が金属元素
④ 約1/3 が非金属元素
⑤ 約1/5が金属元素
⑥ 約1/5が非金属元素
問4 空所〔 4 〕に当てはまる最も適当なものを,次の中から一つ選びなさい。
① 1
② 2
③ 3
④ 4
⑤ 5
⑥ 6
⑦ 7
⑧ 8
□答え……
問1……⑤ 結晶中のすべての原子に共有されている
問2……④ 電気伝導性
問3……① すべて金属元素
問4……4
■2011年 岐阜大学 医 応用生物科 工 一部改
元素は典型元素と遷移元素に分けられる。典型元素では,原子番号の増加とともに ア の数が周期的に変化するので,同一周期中の元素の化学的性質は周期的に変化する。一方,遷移元素は,原子番号が変わっても ア の数があまり変化しない。
問1.文中の ア に適切な語句を答えよ。
問2.原子番号が1~36までの元素に関する以下の記述のうち,正しいものをすべて選び記号で答えよ。
(a) 典型元素はすべて非金属元素である。
(b) 遷移元素はすべて金属元素である。
(c) 遷移元素は10種類ある。
(d) 単体が常温で気体の元素は9種類ある。
(e) 単体が常温で液体の元素は2種類ある。
(f) 原子量は原子番号に常に比例している。
□答え……
問1.……ア 価電子
問2.……(b),(d)
■2012年 広島市立大学 情報科
問 文中のア,イに適切な数字または語句を答えよ。
金属元素の単体は,液体の( ア )を除きすべて常温で固体である。典型元素は,金属元素と非金属元素からなる。一方,周期表の第4周期以降の3族からエ( イ )までの遷移元素は,すべて金属元素である。遷移元素のイオンや化合物は着色しているものが多い。
□答え……
ア……臭素
イ……11
■2011年 三重大学 医 工 生物資源
周期表の ウ 族から11族に属する元素を遷移元素という。このように,典型元素と異なり,(b)遷移元素では周期表の隣接する エ の元素で性質が類似することも多い。
遷移元素では複数の酸化数をとり,有色のイオンを作るものが多い。鉄イオンには+2と+3の酸化数をとる2種類が存在し,鉄(Ⅱ)イオン水溶液は オ 色,鉄(Ⅲ)イオン水溶液は カ 色である。また,遷移元素は(c)錯イオンを作りやすい。錯イオンとは中心となる金属イオンに,非共有電子対をもつ分子や陰イオンが キ 結合したものである。
問1 文章中の, エ ~ カ に適切な語句を,次の①~⑦からそれぞれ選べ。
① 高 い② 低 い③ 上 下④ 左 右
⑤ 赤 褐⑥ 黄 褐⑦ 淡 緑
問2 文章中の イ , ウ に適切な数値を記せ。
問3 文章中の キ , ク に適切な語句を記せ。
問4 下線部(b)の理由を説明せよ。
□答え……
問1
エ……④
オ……⑦
カ……⑥
問2
イ……4
ウ……3
問3
キ……配位
ク……不動態
問4 遷移元素では,原子番号が増加しても価電子の数が1~2で変化しないため。
■2013年 横浜国立大学 理工
次の文章を読み,以下の1)~3)に答えよ。
一般的な金属では,外部からの力によって原子の層が滑るように動き,金属の変形が起きる。金属をたたくと薄く広がる性質を E とよび,引っ張ると細い線にできる性質を F という。この性質を利用して,銅線などが作られる。また,金属は原子半径が G ほど,また価電子数が H ほど金属結合が強くなり,融点や沸点が I なる。一般に,典型元素の金属より遷移元素の金属の方が融点や沸点が J ,密度の K ものが多い。
金属は様々な添加物を加え高機能化させる場合もある。例えば,青銅は金属銅を主成分として L を含む合金であり,美術品や10円硬貨などに用いられる。また,真ちゅう(黄銅と呼ばれることもある)は金属銅を主成分として M を含む合金であり,楽器などに用いられる。
1) EおよびFにあてはまる語句を答えよ。
2) G~Kに該当する語句を下記の語群から選べ。
Gの語群:大きい,小さいHの語群:多い,少ない
Iの語群:高く,低くJの語群:高く,低く
Kの語群:大きい,小さい
3) LおよびMにあてはまる物質名もしくは元素記号を答えよ。
□答え……
1)
E 展性
F 延性
2)
G 小さい
H 多い
I 高く
J 高く
K 大きい
3)
L すず [Sn]
M 亜鉛 [Zn]
--------------------------------------------
無機化学と有機化学の参考書は、下記DLマーケットにて販売しています。
【「くらべてつなげてまとめる無機化学」 第一部】

【「くらべてつなげてまとめる無機化学」 第二部】

【「くらべてつなげてまとめる有機化学」 第一部】

【「くらべてつなげてまとめる有機化学」 第二部】

拙著
『くらべてつなげてまとめる数学 (数学Ⅰ,A,Ⅱ,Bをネットワークでつなぐ)/文英堂』

¥1,296
Amazon.co.jp
も宜しくお願い致します。
↓ランキングが見れます。↓ぽちっとお願いします。

にほんブログ村
↓ランキングが見れます。↓

にほんブログ村
二段滴定・逆滴定に関する問題 完全攻略チャート&過去問解説集
お待たせしました!
『二段滴定・逆滴定に関する問題 完全攻略チャート&過去問解説集』
がやっと完成しました。
二段滴定・逆滴定の問題は受験生が最も苦手とする分野の1つでしょう。
特に、二段滴定となると正答率がかなり落ちてしまいます。
その主な理由として、次の3つが挙げられます。
① 二段滴定とは何かがわかっていない。
② 二段滴定で出題される水溶液がほぼ3つに限られることがわかっていない。
③ 3つの水溶液の二段階の反応式と量的関係が書けない。
二段滴定は、この3つがしっかり頭に入っていれば、さほど難しくはありません。
二段滴定の反応式は…ほとんどの参考書には載っていませんが、「あること」に気づけば、
かなり楽に覚えることができるのです!
本チャートでは、二段滴定・逆滴定の解法を表や図を使うなど、手間暇を惜しまず、かみ砕いてわかりやすく解説しています。
これを見れば、誰でも確実に理解できるようになるでしょう!
では、少し解説していきます。
■二段滴定とは?
水酸化ナトリウムNaOH水溶液に二酸化炭素CO2を吸収させていくと,次のように反応し,少しずつ炭酸ナトリウムNa2CO3に変わっていきます。
2NaOH + CO2 → Na2CO3 + H2O
つまり,NaOH水溶液は,まずは,NaOH・Na2CO3混合水溶液になり,やがて,Na2CO3水溶液に変わります。
さらに,Na2CO3水溶液に,CO2を吸収させていくと,次にように反応し,少しずつ炭酸水素ナトリウムNaHCO3水溶液に変わっていきます。
Na2CO3 + CO2 + H2O → 2NaHCO3
つまり,Na2CO3水溶液は,まずは,Na2CO3・NaHCO3混合水溶液になり,NaHCO3水溶液に変わります。
NaOH水溶液は強塩基性で,Na2CO3水溶液は比較的強い塩基性,NaHCO3水溶液は弱い塩基性を示します。
よって,これらの水溶液すべては塩基性を示すので,いずれも酸である塩酸HClと中和反応します。
そして,これらの中和反応は,滴定曲線中に,pHが急激に変化する部分(中和点)を2か所もつことから,二段(階)滴定(二段階中和)とよばれます。
ここで,NaOH・Na2CO3混合水溶液,Na2CO3水溶液,Na2CO3・NaHCO3混合水溶液の3つの水溶液が登場しました。
二段滴定は、まさに、この3つの水溶液について出題されるのです!
まとめると
Ⅰ.NaOH・Na2CO3混合水溶液タイプ
Ⅱ.Na2CO3水溶液タイプ
Ⅲ.Na2CO3・NaHCO3混合水溶液タイプ
の3つです。
特に,「Ⅰ.NaOH・Na2CO3混合水溶液タイプ」が最も多く出題されるのでしっかりマスターしましょう!
■逆滴定とは?
気体は,液体と異なり体積を測るのは困難(当然,中和滴定できない!)となります。
そこで,気体(例えば,タンパク質の分解により生ずるアンモニアNH3)を滴定するためには,滴定する気体に対して過剰の標準溶液(例えば,NH3ではH2SO4などの酸)に完全に吸収させ,
標準溶液の過剰分を第2の標準溶液(NH3の場合は,余っているのが酸だからNaOHなどの塩基を用いる)で滴定し,物質量を決定します。
このように,通常の中和滴定と異なり,酸(塩基)を滴定するのに塩基(酸)を用いておらず,このような滴定方法を逆滴定といいます。
逆滴定に関する計算問題は,下記,アンモニアの定量と二酸化炭素の定量の2つのタイプをおさえればよいでしょう。
Ⅰ.アンモニアNH3の定量タイプ
Ⅱ.二酸化炭素CO2の定量タイプ
本完全攻略チャートでは、
各滴定の流れ、計算問題の解法をわかりやすくまとめています。
過去問解説集は下記の大学を解説しています。
□収録出題校
慶應大学(2013年),長崎大学(2013年),鹿児島大学(2013年),首都大学(2013年),上智大学(2012年),滋賀医科大学(2012年),三重大学(2012年),岡山大学(2012年),徳島大学(2012年),同志社大学(2011年 2009年),岩手大学(2009年),大阪薬科大学(2009年),甲南大学(2009年)
どの参考書よりもわかりやすく解説しています。
絶対に損はさせません!
これらを圧倒的にわかりやすくまとめています。
これ以上わかりやすく丁寧に解説したチャート&過去問題解説集は他にはどこにもないでしょう!
問題のみはココでみれます。
(完全攻略チャート7枚 過去問解説集21枚 A4普通紙 全28枚)
商品はHP「恋する化学」からご購入いただけます。
拙著
『くらべてつなげてまとめる数学 (数学Ⅰ、A、Ⅱ、Bをネットワークでつなぐ)/文英堂』
¥1、296
Amazon.co.jp
も宜しくお願い致します。
無機化学と有機化学の参考書は、下記DLマーケットにて販売しています。
【「くらべてつなげてまとめる無機化学」 第一部】
【「くらべてつなげてまとめる無機化学」 第二部】
【「くらべてつなげてまとめる有機化学」 第一部】
【「くらべてつなげてまとめる有機化学」 第二部】
↓ランキングが見れます。↓
にほんブログ村
↓ランキングが見れます。↓
にほんブログ村
基本・標準問題を数問解いて、わかった気になっているのが一番危険!
受験生の皆さん、暑い日が続きますが、
勉強の方は、はかどっていますか?
何度もこのサイトで力説していますが、
化学の受験対策で最も効果的な方法は、「自分が志望する大学とその大学と同等レベルの大学の過去問題を数多く繰り返し解くこと」です。
例えば、学校の授業で「浸透圧」の分野を勉強したとします。
そうしたらまずは、学校で与えられている問題集の基本・標準問題を解き、解法の概要・流れを徹底的に頭に叩き込みます。
次は、ココがポイント!
自分が志望する大学とその大学と同等レベルの大学の過去問題から「浸透圧」の分野の問題を探し出し、数多く解きます。
このとき、実際の入試問題と同様に時間をはかって解くとよいでしょう。
はっきり言って、これが最も効率がよく、確実に力がつく方法です!
基本・標準問題をたった数問解いて、わかった気になっているのが一番危険なのです!
「化学は得意さ!」と自信満々で、実際の入試問題を解こうとしたら、
「えっ… あれっ… 解けない……」
と冷や汗をかいた経験はありませんか?
市販されている参考書や問題集に載っている問題は、基本・標準レベルがほとんどなので、実際に出題されている入試問題とのレベルがかけはなれていることがあったりします。
さらに、入試問題の内容も年々進化し、多種多様化しています。
そりゃそうでしょう。
問題作成者は、過去と同じような問題をただ数値をかえて出すわけにはいきません。
なので、
問題集に載っている古~い過去問題を2・3問解いただけでは、太刀打ちできないのです!
とにかく、過去問題をいっぱい解いてください!
しか~し!!!!!
受験生は、分野ごとに、自分が志望する大学とその大学と同等レベルの大学の過去問題
を数多く解くことは、時間、手間暇、金銭の問題などから難しいでしょう。
そこで、宣伝で恐縮ですが…
私が制作販売している
『完全攻略チャート&過去問題解説集』
をうまく活用してほしいのです。
『完全攻略チャート』は、市販されている参考書、予備校や塾のテキスト、どれよりも、わかりやすく解説しています。
なぜなら!
市販されている参考書、予備校や塾のテキスト、DVDを買い集め(その数300点以上)、徹底的に分析し、いいとこどりして、まとめているからです!
そして
『過去問題解説集』
は、近々の難問・良問を数多く収録し、図や色を数多く使用(イラストレーターという描画ソフトを使うことでこれを可能にしています)し、これでもかというくらいにわかりやすく解説しています!
過去問題集解説集のサンプルは、コチラです。
※もっとサンプルが見たいという方は遠慮なく連絡ください。
完全攻略チャートもホームページ『恋する化学』で一部公開しています。
この時期が勝負です!
苦しく逃げ出したくなることもあるでしょうが、
この時期に歯を食いしばり、努力した経験が、将来の自分を支えてくれます!
一日一日、今に集中してがんばってください。
商品はHP「恋する化学」からご購入できます。
拙著
『くらべてつなげてまとめる数学 (数学Ⅰ、A、Ⅱ、Bをネットワークでつなぐ)/文英堂』
¥1、296
Amazon.co.jp
も宜しくお願い致します。
無機化学と有機化学の参考書は、下記DLマーケットにて販売しています。
【「くらべてつなげてまとめる無機化学」 第一部】
【「くらべてつなげてまとめる無機化学」 第二部】
【「くらべてつなげてまとめる有機化学」 第一部】
【「くらべてつなげてまとめる有機化学」 第二部】
↓ランキングが見れます。↓
にほんブログ村
↓ランキングが見れます。↓
にほんブログ村
COD測定って何?薬科大学、薬学部を受ける方は必見!
酸化還元の滴定に関する分野で登場するCOD測定とは何か知っていますか?
COD測定は水質検査に関する問題で、教科書や参考書では取り上げられないことが多いですが、90年代以降よく出題されるようになりました。
90年代以降、東京大学、早稲田大学、慶應義塾大学、北海道大学、お茶の水大学、明治大学、上智大学、香川大学、青山学院大学などなど
難関大学で出題されています。
特に薬科大学、薬学部を受ける方は、きちんとおさえた方がいいでしょう。
2013年では大阪薬科大学、神戸薬科大学などで出題されています。
では、
COD(化学的酸素要求量 Chemical Oxygen Demand)とは、なんなのか解説したいと思います。
CODは簡単に言うと、河川や湖沼の水がどのくらい汚染されているかを表す一つの数値です。
その汚染具合をどう評価するのか?
試料水(例えば、川の水)に含まれている有機物の量を測定します。
その結果…
有機物の量が多いほど汚染されていると評価できる!
なぜ?
河川や湖沼の汚染の主な原因は、家庭排水等による有機物で、有機物が多いと酸素がその有機物を酸化するために消費されてしまう。
その結果、酸素が必要な水中の生物(微生物、水生植物、魚類等)が生息できなくなるからです。
もう少しCODを厳密に解説すると……
CODとは、試料水中の有機化合物を過マンガン酸カリウムKMnO4のような酸化剤で酸化分解したときに使われる酸化剤の消費量を、酸素を酸化剤として用いた場合の酸素の量[mg/L]に換算した値です。つまり、CODの単位は試料水1L当たりの酸素消費量[mg]で表されます。
有機物は還元剤(←ココポイント!)です。よって、直接、酸化剤である酸素で酸化すればいいんじゃない?
しかし…
① 酸素は気体なので、液体のように滴定できない。(逆滴定する方法はある。)
② 当量点で色が変化しない。
③ めちゃくちゃ弱い酸化剤。
なので、酸化剤として使えないのです!!
そこで!
① 液体である。
② 当量点で色が変化する。
③ 強い酸化剤である。
→ これらをすべて満たす万能選手!過マンガン酸カリウムを用います。
入試で登場するのは、ほとんどが過マンガン酸カリウムですが、まれにニクロム酸カリウムK2Cr2O7などが用いられることもあります。
では、用いた過マンガン酸カリウムをどうやって、酸素の量に換算するか?
1molの過マンガン酸カリウムは、下記の半反応式より
5molのe-を受け取ります。
MnO4- + 8H+ + 5e- → Mn2+ + 4H2O
一方、1molの酸素は、下記の半反応式より
4molのe-を受け取ります。
O2 + 4H+ + 4e- → 2H2O
よって、
1molの過マンガン酸カリウムは、5/4molの酸素に相当します。
最後は…
酸素の物質量を試料水1Lあたりのmg数に換算すればOKです。
いかがでしょうか?
おそらく、なんとなくはわかったけど…
という感じだと思います。
これらを確実に理解するには、過去問題を解きながら身につけることが早道です。
COD測定に関する問題 完全攻略チャート&過去問題解説集では、COD測定の解法を色や図を使うなど、かみ砕いてわかりやすく解説しています。
□収録出題校
香川大学(2013年)、奈良県立大学(2013年)、大阪薬科大学(2013年)、神戸薬科大学(2013年)、東京理科大学(2010年)、岐阜大学(2009年)
これ以上わかりやすく丁寧に解説したチャート&過去問題解説集は他にはどこにもありません。
問題のみはココでみれます。
商品はHP「恋する化学」からご購入いただけます。
拙著
『くらべてつなげてまとめる数学 (数学Ⅰ、A、Ⅱ、Bをネットワークでつなぐ)/文英堂』
¥1、296
Amazon.co.jp
も宜しくお願い致します。
無機化学と有機化学の参考書は、下記DLマーケットにて販売しています。
【「くらべてつなげてまとめる無機化学」 第一部】
【「くらべてつなげてまとめる無機化学」 第二部】
【「くらべてつなげてまとめる有機化学」 第一部】
【「くらべてつなげてまとめる有機化学」 第二部】
↓ランキングが見れます。↓
にほんブログ村
↓ランキングが見れます。↓
にほんブログ村
医・歯・薬系大学志望の方、必見!アミノ酸の等電点に関する問題
アミノ酸の等電点に関する問題は、非常によく出題されています。
2013年の過去問題を調べてみると…
北里大学 医
神戸薬科大学 後期 薬
昭和大学 歯 薬 保健医療
中央大学 理工
東京薬科大学
東京理科大学 薬
東邦大学 1次 医
日本医科大学 1次 医
福岡大学 理 工 医 薬
星薬科大学
旭川医科大学 後期日程 医
京都大学 総合人間 教育 理 医 薬 工 農
群馬大学 理工-昼 理工
埼玉大学 後期日程 理 工
東京工業大学 理 工
新潟大学 後期 教育 理 医 歯 工 農
広島大学 総合科 教育 理 医 歯 薬 工 生物
北海道大学 総合教育 医 歯 獣医 水産
と医・歯・薬系大学での出題が目立ちます。
医・歯・薬系大学志望者は、しっかりおさえましょう!
それでは、少し解説したいと思います。
アミノ酸は、一般式RCH(NH2)COOHで表され、アミノ基(-NH2))とカルボキシ基(-COOH)の両方をもつ化合物で、この2つの基が同じ炭素原子に結合しているアミノ酸をα-アミノ酸といいます。
生体中のタンパク質を構成するα-アミノ酸は約20種類あり、それらがペプチド結合によって長くつながってできた高分子化合物がタンパク質です。
アミノ酸は側鎖(-R)の構造により、中性アミノ酸、酸性アミノ酸、塩基性アミノ酸に分類されます。
下記が入試でよく登場する代表的なα-アミノ酸です。
グリシン、アラニンの2つは名称と構造を確実に覚え、それ以外は、硫黄原子やベンゼン環を含むか、中性・酸性・塩基性のどれになるかは最低限覚えましょう!
アミノ酸を水に溶かすと、双性イオンのまま溶けます。
そして、弱酸由来の-COO-や弱塩基由来の-NH3+が存在するため、独立に加水分解を起こし、次のような平衡状態になります。(Rの電離は考えないとする。)
上記の平衡は、次のようにpHによって、陽イオン、双性イオン、陰イオンの比率が変化します。
pHがある値になると、アミノ酸の平衡混合物の電荷が全体として0になります。
このときのpHを等電点といい、それぞれのアミノ酸は固有の等電点を持ちます。
酸性アミノ酸の等電点 → 酸性付近 例:グルタミン酸 3.0
中性アミノ酸の等電点 → 中性付近 例:グリシン 6.0
塩基性アミノ酸の等電点 → 塩基性付近 例:リシン 10.0
★等電点のポイントは、次の2つをおさえましょう!
・等電点では、大部分が双性イオンとして存在し、わずかに残る陽イオンと陰イオンの濃度は、必ず等しくなる。
・等電点の左側(pHが小さい側)では、陽イオンが多く(アミノ酸全体の電荷は+)、右側では、陰イオンが多く(アミノ酸全体の電荷は-)存在する。
等電点に関する問題は、計算問題がよく出題され難しいと思われがちですが、理解してしまえば非常に簡単です。
また、出題されるアミノ酸もグリシンとアラニンが大半を占め、この2つの等電点の求め方は全く同じになります。
「等電点に関する問題チャート&過去問完全攻略チャート」では、等電点の解法を色や図を使うなど、かみ砕いてわかりやすく解説しています。
□収録出題校
新潟大学(2013年)、神戸薬科大学(2013年)、中央大学(2013年)、東京薬科大学(2013年)、早稲田大学(2011年)、徳島大学(2011年)
これ以上わかりやすく丁寧に解説したチャート&過去問題解説集は他にはどこにもありません。
問題のみはココでみれます。
商品はHP「恋する化学」からご購入いただけます。
今すぐpdfデータをほしい方は、下記よりご購入いただけます。
拙著
『くらべてつなげてまとめる数学 (数学Ⅰ、A、Ⅱ、Bをネットワークでつなぐ)/文英堂』
¥1、296
Amazon.co.jp
も宜しくお願い致します。
無機化学と有機化学の参考書は、下記DLマーケットにて販売しています。
【「くらべてつなげてまとめる無機化学」 第一部】
【「くらべてつなげてまとめる無機化学」 第二部】
【「くらべてつなげてまとめる有機化学」 第一部】
【「くらべてつなげてまとめる有機化学」 第二部】
↓ランキングが見れます。↓
にほんブログ村
↓ランキングが見れます。↓
にほんブログ村
気体の溶解度に関する問題
気体の溶解度は固体の溶解度と異なり、苦手とする人が多い分野です。
その要因として、固体の溶解度は、『一般にある温度で溶媒100gに溶かすことのできる最大限の溶質の質量(g)』と決まっているのに対して、気体の溶解度は、いくつかの表現があり、
求める溶解度が物質量・質量なのか、標準状態での体積なのか、その条件下の体積なのかによって、計算の仕方が変わってくる点が挙げられます。
また、計算問題には大きく2通りの出題タイプがあり、「溶解平衡の前後で物質量が変わらない」ことから方程式を立てて解くタイプをきちんと理解していない人が多いです。
それでは、少し解説したいと思います。
■気体の溶解度と温度の関係
一般に、気体の溶解度は高温になるほど減少します。
これは、液体の温度が上昇すると、溶解している気体分子の熱運動が活発になり、液体分子との分子間力に打ち勝つ気体分子の数が増えるためです。
気体分子の運動エネルギーは、液体に溶けると著しく低下し、その分だけ熱エネルギーに変換されます。
つまり、気体の溶解現象は、次の例のように発熱反応となります。
O2(気) + aq ⇔ O2(aq) + 15.9kJ
よって、ルシャトリエの原理により、高温になれば平衡は吸熱方向(左方向)に移動するので、気体の溶解度は高温ほど減少します。
■ヘンリーの法則
「一定温度で、一定体積の溶媒に溶解する気体の物質量(質量)は、その気体の圧力(分圧)に比例する。」
この法則は、ヘンリーの法則とよばれます。
ヘンリーの法則は、次のように言い換えることができます。
ヘンリーの法則①:
一定温度で、一定体積の溶媒に溶解する気体の物質量・質量は、その気体の分圧に比例する。
ヘンリーの法則②:
一定温度で、一定体積の溶媒に溶解する気体の体積は、同じ圧力のもとで測ったとき、気体の分圧に比例する。
ヘンリーの法則③:
一定温度で、一定体積の溶媒に溶解する気体の体積は、分圧に関係なく一定となる。
■気体の溶解度の計算問題
気体の溶解度の計算問題には、大きく「Ⅰ.溶解量を求めるタイプ」、「Ⅱ.物質量不変タイプ」の2通りのタイプがあります。
Ⅰ.溶解量を求めるタイプ
ヘンリーの法則を用いて、溶解量(物質量、質量、体積)を求めるタイプ。このタイプの解法は、『物質量・質量を求める場合』と『体積を求める場合』を分けて考えるとよい。
Ⅱ.物質量不変タイプ
溶解平衡の前後で気体の物質量が不変であることを用いて解くタイプ
このⅡのタイプをきちんと理解していない人が多いですね。
入試ではよく出題されているのに、参考書や問題集にも載っていないこともあり、
なにそれ?って思った人もいるのではないでしょうか?
下記のような問題です。
『酸素は1.0×105Paのときに,27℃の水1Lに1.0×10-3mol,57℃の水1Lに9.0×10-4mol溶けるものとする。
窒素は1.0×105Paのときに,57℃の水1Lに5.0×10-4mol溶けるものとする。
気体定数は8.3×103Pa・L/(K・mol)とする。ただし,気体はすべて理想気体とし,気体の溶解度と圧力の間にはヘンリーの法則が成り立つものとする。
気体の水への溶解に伴う水の体積変化,および温度変化に伴う水の体積変化,水の蒸気圧は無視できるものとする。また,容器の体積は変化しないものとする。
容積が1.1Lの容器に水1Lと酸素を入れた。容器を密閉したまま27℃に保ち,十分に長い時間静かに放置すると,①容器内の圧力は1.0×105Paで一定となった。次に,容器内の温度を57℃まで昇温させ,十分に長い時間静かに放置すると,②容器内の圧力は再び一定となった。その後,温度を57℃に保ったまま容器内に4.2×10-3molの窒素を加えた。この時,容器内の酸素や水は容器の外に出ないものとする。
十分に長い時間静かに放置すると,③容器内の圧力は再び一定となった。
答えは有効数字2桁で求めよ。
(1) 下線①の状態において,容器内の水に溶けている酸素の物質量を求めよ。
(2) 下線①の状態において,容器内に気体として存在する酸素の物質量を求めよ。
(3) 下線②の状態において,容器内の圧力[Pa]を求めよ。
(4) 下線③の状態において,容器内の圧力[Pa]を求めよ。
青山学院大学(2012 理工学部)』
『気体の溶解度に関する問題 完全攻略チャート&過去問題解説集』
では、「気体の溶解度とはなにか」、「2通りの計算問題の解法」を、色や図を使い、これ以上ないくらいにかみ砕いてわかりやすく解説しています。
□収録出題校
島根大学(2013)、東京理科大学(2013)、兵庫県立大学(2012)、東京慈恵会医科大学(2012)、獨協医科大学(2012)、甲南大学(2012)、青山学院大学(2012)、星薬科大学(2012)、九州大学(2011)、同志社大学(2011)、岐阜大学(2011)
これ以上わかりやすく丁寧に解説したチャート&過去問題解説集は他にはどこにもありません。
問題のみはココでみれます。
商品はHP「恋する化学」からご購入いただけます。
今すぐpdfデータをほしい方は、下記よりご購入いただけます。
拙著
『くらべてつなげてまとめる数学 (数学Ⅰ、A、Ⅱ、Bをネットワークでつなぐ)/文英堂』
¥1、296
Amazon.co.jp
も宜しくお願い致します。
無機化学と有機化学の参考書は、下記DLマーケットにて販売しています。
【「くらべてつなげてまとめる無機化学」 第一部】
【「くらべてつなげてまとめる無機化学」 第二部】
【「くらべてつなげてまとめる有機化学」 第一部】
【「くらべてつなげてまとめる有機化学」 第二部】
↓ランキングが見れます。↓
にほんブログ村
↓ランキングが見れます。↓
にほんブログ村
化学基礎を専攻する文系の人も必見!「物質の三態」
お待たせしました!「物質の三態 完全攻略チャート&過去問解説集」の販売を開始しました。
物質には、固体、液体、気体の3つの状態があり、これらを物質の三態といいます。
物質の三態に関する問題は、知識問題と計算問題に分かれ、計算問題の解法は、市販の参考書には詳しく触れられていないことが多く、苦手としている人がいます。
それでは、解法・ポイントを少し公開しちゃいます。
物質の三態に関する問題は、主に次のⅠ~Ⅳの4つのタイプに分類できます。
Ⅰ.固体・液体・気体に関する知識問題タイプ
Ⅱ.加熱曲線に関する知識問題タイプ
Ⅲ.加熱曲線に関する計算問題タイプ
Ⅳ.状態図に関する知識問題タイプ
Ⅰ.固体・液体・気体に関する知識問題タイプ
は、下記の基本事項をおさえましょう。
■状態変化
・固体が液体になる変化を融解、逆に、液体が固体になる変化を凝固という。
・液体が気体になる変化を蒸発(気化)、逆に、気体が液体になる変化を凝縮(液化)という。
・固体が直接気体に変化、また、気体が直接固体に変化するを昇華という。
・沸騰は、液体の内部からも蒸発が起こる現象をいう。
☆蒸発は温度が沸点に達していなくても起こる!
■状態変化とエネルギー
・融解熱(凝固熱)……
固体1molがすべて融解するときに吸収する熱量で、これは1molの液体がすべて凝固するときに放出する熱量(凝固熱)に等しい。
※一般に、粒子間にはたらく引力の強い物質ほど融点は高く、融解熱も大きくなる。例えば、イオン間にはたらくクーロン力は、分子間にはたらく分子間力よりもかなり強いので、イオン結晶は分子結晶よりも融解熱はかなり大きくなる。
・蒸発熱(凝縮熱)……液体1molがすべて蒸発するときに吸収する熱量で、これは、1molの気体がすべて凝縮するときに放出する熱量に等しい。
・昇華熱……固体1molがすべて昇華するときに吸収する熱量で、これは、1molの気体がすべて固体に変化するときに放出する熱量に等しい。
Ⅱ.加熱曲線に関する知識問題タイプ
については下記をおさえましょう。
下図は氷を加熱していき、水を経て水蒸気に状態変化させるまでの加熱時間と温度変化との関係を表したグラフで加熱曲線とよびます。
加熱曲線に関する知識を問う問題は、主に下記(Ⅰ)~(Ⅲ)の3つのタイプに分類できます。
すべて重要なので確実に覚えましょう!
(Ⅰ) 状態を問う知識問題
① ab間の状態は? 固体のみ。
② bc間の状態は? 固体と液体が共存している。
③ cd間の状態は? 液体のみ。
④ de間の状態は? 液体と気体が共存している。
⑤ ef 間の状態は? 気体のみ。
(Ⅱ) 名称を問う知識問題
① 温度tA℃は何というか? 融点
② 温度tB℃は何というか? 沸点
③ bc間で1molの物質が吸収する熱量は何というか? 融解熱
④ de間で1molの物質が吸収する熱量は何というか? 蒸発熱
(Ⅲ) 理由・記述問題
① bc間では加熱しているのにもかかわらず温度が上昇しない理由は?
融解中は加熱によって加えられたエネルギーは、固体の結晶配列を崩すために使われるので温度上昇は起こらない。
② de間では加熱しているのにもかかわらず温度が上昇しない理由は?
沸騰中は加熱によって加えられたエネルギーは、液体の粒子間にはたらく引力をすべて切断するために使われるので温度上昇は起こらない。
③ 一般に、蒸発熱は融解熱より大きくなる理由は?
融解熱は、分子間にはたらく結合の一部を切るのに必要なエネルギーであるが、 蒸発熱は、その結合を完全に切断にしたうえで、分子間の距離をさらに大きくするために必要なエネルギーである。このため蒸発熱のほうが大きなエネルギーとなる。
Ⅳ.状態図に関する知識問題タイプ
については下記をおさえましょう。
純物質は、それぞれの温度・圧力ごとに、その三態(固体・液体・気体)が決まっています。
純物質が様々な温度・圧力においてどのような状態であるかを示した図を物質の状態図(状態図は物質ごとに固有の形を示す)といいます。
図1は水H2O、図2は二酸化炭素CO2の状態図です。
状態図に関する知識を問う問題は、主に下記(Ⅰ)~(Ⅲ)の3つのタイプに分類でます。
(Ⅰ) 名称を問う知識問題
① 点Aの名称は? 三重点
② 点Bの名称は? 臨界点
③ 曲線ABの名称は? 蒸気圧曲線
④ 曲線ACの名称は? 融解曲線
⑤ 曲線OAの名称は? 昇華圧曲線
⑥ 状態がⅢ→Ⅰに変化するときの状態変化の名称は? 蒸発
⑦ 状態がⅡ→Ⅰに変化するときの状態変化の名称は? 昇華
⑧ 状態がⅡ→Ⅲに変化するときの状態変化の名称は? 融解
(Ⅱ) 状態を問う知識問題
① Ⅰの領域の状態は? 気体
② Ⅱの領域の状態は? 固体
③ Ⅲの領域の状態は? 液体
④ 曲線AB上での状態は? 液体と気体が共存している。
⑤ 曲線AC上での状態は? 液体と固体が共存している。
⑥ 曲線OA上での状態は? 固体と気体が共存している。
⑦ 点Aでの状態は? 固体、液体、気体が共存している。
⑧ 点Bでの状態は? 液体と気体が区別できない状態。
(Ⅲ) 理由・記述問題
① H2Oの状態図において(a)を出発点として、温度を一定にしたまま圧力を加えていくと、状態はどのようになるか?
水の融解曲線の傾きは負なので、温度を一定にして圧力を上げると図中Ⅲの領域に達する。つまり、固体から液体に状態変化する。
② CO2の状態図において(b)を出発点として、温度を一定にしたまま圧力を加えていくと、状態はどのようになるか?
CO2の融解曲線の傾きは正なので、温度を一定にして庄力を上げても固体のままである。
③ 圧力を上げると、H2O、CO2の沸点・融点はどうなるか?
図1のH2Oの状態図では、Tから圧力を大きくしていくと、融解曲線の傾きは負で蒸気圧曲線の傾きは正であるため、圧力増加とともに融点は下がり、沸点は高くなる。図2のCO2の状態図では、Tから圧力を大きくしていくと、融解曲線も蒸気圧曲線も傾きは正であるため、圧力増加とともに 融点・沸点はともに高くなる。
Ⅲ.加熱曲線に関する計算問題タイプ
については、「物質の三態 完全攻略チャート&過去問題解説集」の中で詳しく解説しています。
過去問解説集の収録校は下記になります。
中京大学(2013)、徳島大学(2013)、金沢大学(2013)、明治大学(2013、2012)、東京理科大学(2013)、東京医科歯科大学(2012)、山形大学(2012)、広島大学(2012)、弘前大学(2012)、防衛大学校(2011)
本チャートでは、知識・計算問題の両方が確実に解けるようになるようにどの参考書よりもわかりやすく解説しています。
百聞は一見に如かずです!!
物質の三態は、化学基礎の範囲に含まれているため、センター試験を受ける文系の人も必須です。
問題のみはココみれます。
商品はHP「恋する化学」からご購入いただけます。
今すぐpdfデータをほしい方は、下記よりご購入いただけます。
拙著
『くらべてつなげてまとめる数学 (数学Ⅰ、A、Ⅱ、Bをネットワークでつなぐ)/文英堂』
¥1、296
Amazon.co.jp
も宜しくお願い致します。
無機化学と有機化学の参考書は、下記DLマーケットにて販売しています。
【「くらべてつなげてまとめる無機化学」 第一部】
【「くらべてつなげてまとめる無機化学」 第二部】
【「くらべてつなげてまとめる有機化学」 第一部】
【「くらべてつなげてまとめる有機化学」 第二部】
↓ランキングが見れます。↓
にほんブログ村
↓ランキングが見れます。↓
にほんブログ村
覚える時間・労力を大幅に短縮!「コロイドに関する問題 完全攻略チャート&過去問題解説集」
コロイドに関する問題はほとんどが知識問題なので覚えれば確実に点数になります。
しかし、覚えることが多かったり似たような用語(「凝析、塩析、透析」、「正コロイド、負コロイド、親水コロイド、疎水コロイド、保護コロイド」…などなど)が多いため、何ををどうやって覚えたらいいのか苦労している人が多いのではないでしょうか?
それでは、ポイントを解説したいと思います。
コロイドとは、コロイド粒子が分散した状態のことをいい、直径約10-9~10-7m(10-7~10-5cm)程度の大きさをもつ粒子をコロイド粒子といい、コロイド粒子が液体中に分散したものをコロイド溶液(ゾルともよぶ)いいます。
すべてのコロイド粒子は正または負の電荷をもちます。
コロイドに関する入試問題は、大きく4つのタイプに分類できます。
Ⅰ.コロイドの大きさに関する問題
Ⅱ.ゾルとゲルに関する問題
Ⅲ.コロイドの分類に関する問題
Ⅳ.コロイド溶液の性質に関する問題
それでは、それぞれのポイントを下記に列挙します。
Ⅰ.コロイドの大きさに関する問題
・コロイド粒子の直径は、約10-9~10-7m(10-7~10-5cm)で、ろ紙は通過できるが、セロハン(半透膜)は通過できない。
・コロイド粒子は、光学顕微鏡では観察することができないが、限外顕微鏡では観察できる。
★ポイント
ろ紙の穴>コロイド粒子>セロハン(半透膜)の穴
限外光学顕で観察できる。光学顕微鏡で観察できない。
Ⅱ.ゾルとゲルに関する問題
・流動性をもったコロイド溶液をゾル、流動性を失った半固体状のコロイドをゲル(例:ゆで卵、豆腐、寒天、こんにゃく、ゼリー)、ゲルを乾燥させた固体をキセロゲル(例:シリカゲル、高野豆腐)という。
★ポイント
流動性をもつ → ゾル
流動性を失って固まったもの → ゲル
ゲルを乾燥させた固体 → キセロゲル
Ⅲ.コロイドの分類に関する問題
コロイドの分類には、主に以下のように4つの分類があります。
これらを整理して覚えましょう!
ⅰ.コロイドの状態による分類
・コロイド粒子を分散させている物質を分散媒、コロイド粒子として分散している物質を分散質という。
・分散媒が液体のもののうち、分散質が固体のものを懸濁液(けんだくえき),液体のものを乳濁液という。
ⅱ.コロイドの構造による分類
・デンプンやタンパク質のように1個の分子がコロイド粒子の大きさのものを分子コロイドという。
デンプン分子がコロイドとしてふるまう理由は、デンプン分子は表面に多数のヒドロキシ基をもつので、これが多数の水分子を引き付けるため。セッケン分子のようにいくつかの分子が集合体(ミセル)をつくったものを会合コロイド(ミセルコロイド)という。
※分散コロイドもあるが、入試ではほとんど問われないので省略。
ⅲ.コロイドの性質(水和性)による分類
1.水との親和力が小さく、少量の電解質水溶液を加えると、容易に沈殿しやすいコロイドを疎水コロイドという。疎水コロイドには、主に無機化合物が多く金、銀、白金、硫黄、Fe(OH)3、Al(OH)3などがある。
2.水との親和力が大きく、少量の電解質水溶液を加えても沈殿しないコロイドを親水コロイドという。親水コロイドは、-OH、-COOH、-NH2などをもち、水和により安定化されている。
親水コロイドには、主に有機化合物が多く、ゼラチン、デンプン、セッケンのミセル、タンパク質、にかわ、寒天などがある。
3.疎水コロイドに親水コロイドを加えると、疎水コロイドは親水コロイドの粒子に取り囲まれ、凝析しにくくなる。このような働きをもつ親水コロイドを保護コロイドという。
ⅳ.コロイドの性質(電気的)による分類
・コロイド粒子は分子やイオンに比べて質量が大きいので、沈殿しそうに思えるが、電荷をもつため、互いに反発し合って長時間安定に存在している。
すべてのコロイド粒子は正または負の電荷をもち、正に帯電したコロイドを正コロイド、負に帯電したコロイドを負コロイドという。
正コロイドには、Fe(OH)3、Al(OH)3、負コロイドには硫黄、粘土、金、白金などががある。
★ポイント
一般に、金属の水酸化物のコロイドは正コロイド
Ⅳ.コロイド溶液の性質に関する問題
は下記6つのタイプがあります。
ⅰ.チンダル現象に関する問題
ⅱ.ブラウン運動に関する問題
ⅲ.凝析に関する問題
ⅳ.塩析に関する問題
ⅴ.電気泳動に関する問題
ⅵ.水酸化鉄(Ⅲ)の生成と透析に関する問題
解説はここまでとします。
本チャートでは、どの用語が出題されているのか、過去問題を徹底的に分析し、いかに楽に覚えるかにこだわりました。
ここまで時間をかけてデータを集め分析している人はほとんどいないでしょう。
オリジナルの語呂合わせ暗記法も多数載せています。
どの参考書よりもわかりやすくまとめていることを保証します!
本チャートで勉強すれば圧倒的に覚える時間、労力を短縮できます!!
過去問題も20大学、センター試験と盛り超沢山!
■収録出題校
筑波大学(2013、近畿大学(2011)、立教大学(2013)、神戸薬科大学(2013)、愛知医科大学(2013)、琉球大学(2013)、昭和大学(2013)、昭和薬科大学(2013)
静岡大学(2013)、関西学院大学(2013)、日本大学(2012)、県立広島大学(2012)、東京都市大学(2012)、東邦大学(2012、2011)、順天堂大学(2012)、北海道薬科大学(2011)、京都薬科大学(2011)、近畿大学(2011)、成蹊大学(2011)、千葉大学(2009)、センター試験(2015 本試験)、センター試験(1993 本試験)一部改、センター試験(1994 本試験)一部改
A4普通紙 4枚(チャート)+21枚(過去問題解説集) 全25枚
問題のみはココみれます。
商品はHP「恋する化学」からご購入いただけます。
今すぐpdfデータをほしい方は、下記よりご購入いただけます。
拙著
『くらべてつなげてまとめる数学 (数学Ⅰ、A、Ⅱ、Bをネットワークでつなぐ)/文英堂』
¥1、296
Amazon.co.jp
も宜しくお願い致します。
無機化学と有機化学の参考書は、下記DLマーケットにて販売しています。
【「くらべてつなげてまとめる無機化学」 第一部】
【「くらべてつなげてまとめる無機化学」 第二部】
【「くらべてつなげてまとめる有機化学」 第一部】
【「くらべてつなげてまとめる有機化学」 第二部】
↓ランキングが見れます。↓
にほんブログ村
↓ランキングが見れます。↓
にほんブログ村
2次試験対策は本当に大丈夫ですか?
化学は得意だと思っていたけれど、模試や過去問を解いてみたら、思うような点数を取れなかったというような経験はありませんか?
その理由の1つは、入試レベルの問題を数多くを解いていなかったことが挙げられます。
書店に並んでいる参考書や問題集に掲載されている問題は、ほとんどが基本から標準問題で、問題数も各分野、各テーマで数問程度です。
はっきり言って、それだけ解いただけでは、医歯薬系、中堅以上の私立・国公立大学には太刀打ちできません!
「化学は余裕!」なんて思い違いしているそこのあなた!
なめていたら痛い目にあいますよ!
テーマごとにまとめた過去問をアップしたので、是非挑戦してみてください!
今回、期間限定で特別に解答がみたいという方に2点無料で差し上げます!
件名に「解答希望」
メッセージ欄に「氏名 メールアドレス 希望するテーマ」を記載の上、
infoアットマークfastliver.com
まで連絡ください。
■気体の溶解度に関する問題
□収録出題校
島根大学(2013)、東京理科大学(2013)、兵庫県立大学(2012)、東京慈恵会医科大学(2012)、獨協医科大学(2012)、甲南大学(2012)、青山学院大学(2012)、星薬科大学(2012)、九州大学(2011)、同志社大学(2011)、岐阜大学(2011)
■化学結合と結晶の性質に関する問題
□収録出題校
横浜国立大学(2013)、早稲田大学(2013)、立教大学(2013)、慶應義塾大学(2012)、早稲田大学(2011 2013)、日本女子大学(2011)、岐阜大学(2011)、長崎大学(2013)、信州大学(2013)、金沢大学(2012 2013)、三重大学(2011)、東京理科大学(2011 2013 2012)、琉球大学(2012)
■結晶格子に関する問題
□収録出題校
東北大学(2010、2012年)、愛媛大学(2013年)、岩手大学(2013年)、近畿大学(2013年)、佐賀大学(2013年)、鹿児島大学(2013年)、上智大学(2013年)、静岡大学(2009、2010年)、筑波大学(2009、2013年)、島根大学(2009年)、同志社大学(2012年)
■物質の三態
□収録出題校
中京大学(2013)、徳島大学(2013)、金沢大学(2013)、明治大学(2013、2012)、東京理科大学(2013)、東京医科歯科大学(2012)、 山形大学(2012)、広島大学(2012)、弘前大学(2012)、防衛大学校(2011)
■気体の計算問題
□収録出題校
電気通信大学(2011年)、鳥取大学(2011年)上智大学(2012年)、九州大学(2013年)、岐阜大学(2013年)、関西大学(2011年)、杏林大学(2013年)、愛知医科大学(2013年)お茶の水女子大学(2013年)、北海道大学(2012年)
■化学平衡に関する問題
□収録出題校
東京理科大学(2011年)、愛媛大学(2013年)、旭川医科大学(2012年)、関西大学(2010年)、岩手大学(2012年)、 九州工業大学(2012年)、広島大学(2012年)、静岡大学(2013年)、早稲田大学(2011年)、徳島大学(2012年)、北海道大学(2011年)、 同志社大学(2011年)、名古屋大学(2012年)、明治屋大学(2011年)
■二段滴定・逆滴定に関する問題
□収録出題校
慶應大学(2013年)、長崎大学(2013年)、鹿児島大学(2013年)、首都大学(2013年)、上智大学(2012年)、滋賀医科大学(2012年)、三重大学(2012年)、岡山大学(2012年)、徳島大学(2012年)、同志社大学(2011年 2009年)、岩手大学(2009年)、大阪薬科大学(2009年)、甲南大学(2009年)
■電離平衡に関する問題
□収録出題校
東京理科大学(2012年)、早稲田大学(2009年)、昭和大学(2012年)、東京農工大学(2010年)、立命館大学(2009年)、 明治大学(2013年)、高知大学(2012年)、関西大学(2009年、2011年)、長崎大学(2010年)
■酸化還元 COD測定に関する問題
□収録出題校
香川大学(2013年)、奈良県立大学(2013年)、大阪薬科大学(2013年)、神戸薬科大学(2013年)、東京理科大学(2010年)、岐阜大学(2009年)
■電気分解 並列回路に関する問題
□収録出題校
大分大学(2013年)、東京理科大学(2013年)、上智大学(2012年)、青山大学(2012年)、山梨大学(2011年)
■沸点上昇・凝固点降下に関する問題
□収録出題校
慶應義塾大学(2013年)、愛媛大学(2013年)、岩手大学(2013年)、宮崎大学(2010年)、札幌医科大学(2013年)、鹿児島大学(2010年)、昭和大学(2013年)、 静岡大学(2012年)、大阪府立大学(2011年)、東京理科大学(2011年)、東京薬科大学(2012年)
■浸透圧に問題
□収録出題校
東京医科歯科大学(2013年)、広島大学(2013年)、横浜国立大学(2012年)、名古屋市立大学(2012年)、福井大学(2012年)、大阪市立大学(2012年)、東京理科大学(2010年)、中央大学(2010年)、千葉大学(2010年)、埼玉大学(2009年)
■コロイドに関する問題
□収録出題校
筑波大学(2013、近畿大学(2011)、立教大学(2013)、神戸薬科大学(2013)、愛知医科大学(2013)、琉球大学(2013)、昭和大学(2013)、昭和薬科大学(2013) 静岡大学(2013)、関西学院大学(2013)、日本大学(2012)、県立広島大学(2012)、東京都市大学(2012)、東邦大学(2012、2011)、順天堂大学(2012) 北海道薬科大学(2011)、京都薬科大学(2011)、近畿大学(2011)、成蹊大学(2011)、千葉大学(2009)、センター試験(2015 本試験)、センター試験(1993 本試験)一部改、センター試験(1994 本試験)一部改
■溶解度積の計算問題
□収録出題校
東北大学(2009年)、愛知教育大学(2010年)、横浜国立大学(2009年)、岩手大学(2012年)、宮崎大学(2013年)、佐賀大学(2013年)、静岡大学(2009、2012年)、 千葉大学(2010年)、大阪教育大学(2012年)、筑波大学(2013年)、島根大学(2009年)、徳島大学(2012年)、 和歌山大学(2010年)
■芳香族化合物の異性体に関する問題
□収録出題校
旭川医科大学(2012年)、横浜国立大学(2009年)、岡山大学(2013年)、関西大学(2012年)、関西学院大学(2010年)、 京都産業大学(2012年)、近畿大学(2013年)、金沢大学(2012年)、高知大学(2013年)、大阪市立大学(2010年、2013年)、筑波大学(2012年)、 同志社大学(2011年)、立命館大学(2011年)
■芳香族化合物の系統分離に関する問題
□収録出題校
山形大学(2013年)、上智大学(2013年)、琉球大学(2012年)、中央大学(2012年)、立教大学(2012年)、立命館大学(2011年)、大分大学(2011年)、神戸大学(2011年)
■油脂の計算問題
□収録出題校
岐阜大学(2011、2013年)、金沢大学(2011年)、熊本大学(2013年)、弘前大学(2012年)、埼玉大学(2013年)、山形大学(2012年)、 信州大学(2013年)、神戸大学(2012年)、筑波大学(2011年)、富山大学(2010年)、北海道大学(2011年)、名古屋市立大学(2011年)
■アセタール化の計算問題
□収録出題校
長崎大学(2008年)、明治大学(2013年)、法政大学(2012年)、千葉大学(2009年)、神戸薬科大学(2008年、2013年)、神戸学院大学(2011年)、埼玉大学(2013年)、高知大学(2009年)、慶應大学(2011年)、金沢大学(2013年)、岐阜大学(2011年)、愛媛大学(2009年)
■アミノ酸の等電点に関する問題
□収録出題校
新潟大学(2013年)、神戸薬科大学(2013年)、中央大学(2013年)、東京薬科科大学(2013年)、早稲田大学(2011年)、徳島大学(2011年)
■ペプチドの構造決定に関する問題
□収録出題校
群馬大学(2013)、広島大学(2013)、大阪医科大学(2013)、同志社大学(2013)、奈良県立医科大学(2013)、北海道大学(2013)、北里大学(2013)、神戸薬科大学(2012)、早稲田大学(2011)
■医薬品に関する問題
□収録出題校
岐阜大学(2013)、同志社大学(2013)、昭和大学(2013)、信州大学(2013)、大阪医科大学(2013)、富山大学(2012)、東京理科大学(2012)、長崎大学(2012)、大阪市立大学(2012)、広島大学(2012)、岡山大学(2012)、熊本大学(2009 2010)、新潟大学(2011)、立命館(2011)、名城大学(2011)、摂南大学(2009)
■ハロゲンに関する問題
□収録出題校
関西大学(2011年)、金沢大学(2012年)、自治医科大学(2011年)、鹿児島大学(2012年)、上智大学(2011年)、大阪市立大学(2010年)、長崎大学(2010年)、東京慈恵医科大学(2012年)、東京理科大学(2011年)、同志社大学(2012年)、日本大学(2012年)、富山大学(2012年)
■化学工業に関する問題
□収録出題校
横浜市立大学(2012年)、関西学院大学(2012年)、大阪医科大学(2012年)、東海大学(2012年)、 近畿大学(2012年)、中央大学(2012年)、星薬科大学(2012年)、早稲田大学(2012年)、 名古屋大学(2012年)、岐阜大学(2011年)、秋田大学(2011年)、上智大学(2011年)、独協大学2011年)、関西大学(2011年)、首都大学東京(2011年)、信州大学(2011年)、法政大学(2011)、防衛医科大学(2011年)、立教大学(2011年)、和歌山大学(2011年)
■気体の製法と性質に関する問題
□センター試験 収録年
センター本試験 2011年、2010年、2008年、2006年、2003年、2001年、2000年
センター追試験 2010年、2009年、2008年、2007年、2005年、2004年、2002年、2001年、2000年
■金属イオンの確認と性質
□収録出題校
高知大学(2013年)、琉球大学(2011年)、立命館大学(2011年)、中央大学(2011年)、星薬科大学(2011年)、群馬大学(2011年)、甲南大学(2012年)、名古屋市立大学(2012年)、宮崎大学(2012年)
■化学反応の量的計算問題
□収録出題校
センター本試験 本試験:2012年、2011年、2010年、2008年、2005年、2004年、2003年、2002年、2001年、2000年
センター追試験: 2010年、2009年、2006年、2005年
■溶液の濃度に関する問題
□収録出題校
学習院大学(2011年)、熊本大学(2011年)、関西大学(2012年)、和歌山大学(2011年)、福島大学(2011年)、東京理科大学(2011年)、岐阜大学(2011年)、日本女子大学(2011年)
センター試験 本試験:2009本、2007本 追試験: 2009追、2005追、2003追
■固体の溶解に関する問題
□収録出題校
関西大学(2012年)、大阪市立大学(2010年)、学習院大学(2011年)、弘前大学(2012年)、東京理科大学(2012年)、日本大学(2011年 )
センター試験 本試験:2004年、2002年、2000年、1998年、1997年、1995年 追試験:1996年
拙著
『くらべてつなげてまとめる数学 (数学Ⅰ、A、Ⅱ、Bをネットワークでつなぐ)/文英堂』
¥1、296
Amazon.co.jp
も宜しくお願い致します。
無機化学と有機化学の参考書は、下記DLマーケットにて販売しています。
【「くらべてつなげてまとめる無機化学」 第一部】
【「くらべてつなげてまとめる無機化学」 第二部】
【「くらべてつなげてまとめる有機化学」 第一部】
【「くらべてつなげてまとめる有機化学」 第二部】
↓ランキングが見れます。↓
にほんブログ村
↓ランキングが見れます。↓
にほんブログ村
化学 理由を問う記述問題
大学入試の化学の2次試験では、「理由を問う記述問題」がよく出題され合否を分けます!
しかし、どんな理由がよく問われるのか、どのように記述すればいいのか、わかっていない人がほとんどです。
そこで!
国公私立大学の7年分の「理由を問う記述問題」を約3年の月日をかけて徹底的に分析し、頻出・覚えておきたい問題を厳選してまとめました。
はっきり言って、この厳選した問題のテキストだけでも十分に価値がありますが、
受験生にとっては、覚えなければ意味がないので、
ちょっとした時間に繰り返し何度も聴くことで自然に覚えられるように声優さんにお願いして音声ファイル化(mp3形式)しました。
音声ファイルをiPhone等のmp3対応プレイヤーに入れて、通学時間、就寝前等の空いた時間に聴くことで効率的に学習できます!
■具体的な内容紹介
無機化学編……テキスト(問題数51問。14ページ。pdf形式)+音声(録音時間 約26分。51ファイル mp3形式)
有機化学編……テキスト(問題数52問。11ページ。pdf形式)+音声(録音時間 約26分。52ファイル mp3形式)
理論化学編……テキスト(問題数46問。12ページ。pdf形式)+音声(録音時間 約26分。46ファイル mp3形式)
※音声ファイルは、mp3形式で自分で編集できるように1問ごとに分けて収録しています。
※テキストファイルは、問題と解答例(解答は問われる文字数によって変わってきますが、最低限おさえておきたいポイントを含めた解答例としています。)、一部解説つき。
□■□■□■掲載問題一例□■□■□■
◆無機化学
■問題
リチウムと同じアルカリ金属であるカリウムが、リチウムより激しく水と反応する理由は?
■問題
アルカリ金属の単体は、原子番号が大きいほど融点が低くなる理由は?
■問題
水酸化ナトリウムの固体の質量をはかりとっても、正確な濃度の水溶液を調製することができない理由は?
■問題
2族元素の原子が、いずれも2価の陽イオンになりやすい理由は?
■問題
石灰水に二酸化炭素を通すと、白濁する理由は?
■問題
金属カルシウムの融点は、同周期の1族の金属カリウムの融点に比べて極めて高い理由は?
■問題
実験室で二酸化炭素を発生させる時、石灰石に希塩酸を反応させる。このとき、希塩酸の代わりに希硫酸を用いると、気体の発生が途中で停止してしまう理由は?
■問題
硫酸バリウムが、X線撮影の造影剤に使われる理由は?
■問題)
カルシウムの単体をつくるために、カルシウム塩の水溶液を電気分解することが不適当な理由は?
■問題
シリカゲルが乾燥剤や吸着剤に使われる理由は?
■問題
ダイヤモンドは電気を通さないが、黒鉛は電気を通す理由は?
■問題
ダイヤモンドは非常に硬いが、黒鉛はもろい(軟らかい)理由は?
■問題
二酸化ケイ素の固体は、水に溶けにくい理由は?
■問題
リンの同素体である黄リンを水中で保存する理由は?
■問題
アンモニアは、実験室では塩化アンモニウムと水酸化カルシウムの混合物を加熱することで得られる。この製法において、
問題1
試験管の口を水平より下げておく理由は?
問題2
アンモニアは、上方置換によって捕集する理由は?
問題3
アンモニアの乾燥には濃硫酸は不適当である理由は?
■問題
濃硝酸を褐色ビンにいれて冷暗所で保存する理由は?
■問題
窒素は、常温・常圧で化学的に非常に安定である理由は?
■問題
水は16族元素の水素化物の中で異常に高い沸点を示す理由は?
■問題
濃硫酸は酸としての性質はきわめて弱く、希硫酸が強酸性を示す理由は?
■問題
希硫酸を調製する場合、必ず水をかき混ぜながら濃硫酸を少しずつ加えなければいけない理由は?
■問題
ハロゲンの単体は、原子番号が大きいほど融点・沸点が高くなる理由は?
■問題
ハロゲンの単体のうち、フッ素が最も酸化力が強い理由は?
■問題
フッ化水素が他のハロゲン化水素と比較して沸点が著しく高い理由は?
■問題
単体の塩素は酸化マンガン(Ⅳ)に濃塩酸を加えて加熱し、発生する気体を水の入った洗気びんに通して、次に濃硫酸の入った洗気びんに通して捕集します。水と濃硫酸を用いる理由は?
■問題
水酸化鉄(Ⅱ)の沈殿を含む水溶液をそのまま放置すると、沈殿の色が次第に変化して赤褐色になる。この理由は?
■問題
鉄やアルミニウムの単体は塩酸や希硫酸には溶けるが、濃硝酸や熱濃硫酸にはほとんど溶けない理由は?
■問題
鉄を亜鉛でめっきしたものは、鉄をスズでめっきしたものよりさびにくい理由は?
■問題
ブリキ、トタンの表面に傷がついて鉄が露出したとき、ブリキよりもトタンのほうがさびにくい理由は?
■問題
アルミニウムはイオン化傾向が大きいのにもかかわらず、さびが進行しない理由は?
■問題
アルミニウムの合金であるジュラルミンが航空機材料などに用いられる理由は?
■問題
アルミニウムイオンを含む水溶液の電気分解では、アルミニウムの単体を得ることができない理由は?
■問題
アルミニウムの融解塩電解の際に氷晶石を加える理由は?
■問題
硫酸銅(Ⅱ)無水物が水分の検出に用いられる理由は?
■問題
硫化水素は、湿らせた酢酸鉛紙を黒変する理由は?
◆有機化学
■問題
アセチレンに水が付加して生じるビニルアルコールが、すぐにアセトアルデヒドに異性化する理由は?
■問題
メタノール、エタノールが水によく溶ける理由は?
■問題
アルデヒドが銀鏡反応を示す理由は?
■問題
酢酸の水溶液は弱酸性を示すが、無水酢酸の水溶液は中性を示す理由は?
■問題
フマル酸は、マレイン酸より融点が高くなる理由は?
■問題
マレイン酸は加熱すると、分子内脱水して無水マレイン酸が生成する。しかし、フマル酸を加熱しても分子内脱水されない理由は?
■問題
セッケンを水に溶かしたとき、塩基性を示す理由は?
■問題
硬水中で、セッケンの洗浄力が低下する理由は?
■問題
合成洗剤は、硬水中で洗浄力が低下しない理由は?
■問題
セッケンは、絹や羊毛の洗浄には適さない理由は?
■問題
有機化合物を完全に燃焼させて元素分析を行う際に、燃焼によって生成した混合気体を、はじめに塩化カルシウム管に通し、次にソーダ石灰管に通して吸収させる。このとき混合気体を通す順序を逆にしてはいけない理由は?
■問題
ベンゼンを空気中で点火すると、多量のススが出る理由は?
■問題
エチレンの二重結合は付加反応を起こしやすく、ベンゼンの二重結合では、置換反応の方が起こりやすい理由は?
■問題
フェノール類が水に溶けにくい理由は?
■問題
サリチル酸メチル、アセチルサリチル酸のそれぞれに塩化鉄(Ⅲ)水溶液を加えると、サリチル酸メチルだけが呈色した。その理由は?
■問題
安息香酸とフェノールを混合したエーテル溶液に、炭酸水素ナトリウム水溶液を加えてよく撹拌した。静置後、水層とエーテル層に分離したところ、エーテル層にはフェノールのみが含まれていた。この理由は?
■問題
アニリンが塩酸に溶ける理由は?
■問題
アニリンに酢酸を加えて加熱したり、無水酢酸を加えると塩基性を失う理由は?
■問題
アニリンを希塩酸に溶かし、氷で冷却しながら亜硝酸ナトリウム水溶液と反応させるとジアゾ化が起こり、塩化ベンゼンジアゾニウムが生じる。
この反応では、5℃以下に氷冷しながら行う必要がある理由は?
■問題
単糖類や二糖類が水によく溶ける理由は?
■問題
セルロースが水に溶けにくい理由は?
■問題
グルコースの水溶液が還元性を示す理由は?
■問題
デンプンおよびセルロースに、ヨウ素ヨウ化カリウム水溶液を加えた。デンプンは青~青紫色に呈色したが、セルロースは呈色しなかった。その理由は?
■問題
紙(セルロース)に濃硫酸をたらすと真っ黒くなる理由は?
■問題
木綿や麻が吸湿性に優れている理由は?
■問題
木綿や麻が塩基には比較的強く、酸には弱い理由は?
■問題
アミノ酸が水によく溶ける理由は?
■問題
アミノ酸が他の有機化合物に比べて、融点が高い理由は?
■問題
トリペプチドを溶かした水溶液に、水酸化ナトリウム水溶液を加えた後、硫酸銅(Ⅱ)水溶液を少量加えると赤紫色になった。この呈色はジペプチドでは生じない理由は?
■問題
等電点が9.7のリシンを中性の緩衝溶液に溶解し直流電圧をかけると、陰極側に移動する理由は?
■問題
酵素が加熱により、触媒としての機能を失う理由は?
■問題
タンパク質を加熱したり、酸や塩基を加えると凝固する理由は?
■問題
ポリビニルアルコールは、その構造式から見るとビニルアルコールの重合により得られると予測される。しかし実際は、ポリ酢酸ビニルの加水分解により合成されている。その理由は?
■問題
ポリビニルアルコールが水溶性である理由は?
■問題
ポリ塩化ビニルの焼却には注意が必要な理由は?
■問題
高分子化合物の融点は、低分子化合物とは異なり、一般に一定の融点を示さない理由は?
■問題
尿素樹脂やメラミン樹脂を加熱すると硬くなる理由は?
■問題
生ゴム(天然ゴム)の大部分は、トランス形ではなく、シス形のポリイソプレンからなる理由は?
■問題
生ゴム(天然ゴム)の弾性は、空気中に長く放置すると失われる理由は?
■問題
生ゴム(天然ゴム)に5~8%の硫黄を加えて、加熱することで弾性が増す理由は?
◆理論化学
■問題
元素を原子番号の小さい順に並べると、20番目までは性質のよく似た元素が周期的に現れる理由は?
■問題
遷移元素では、族としての類似性のほかに同一周期で隣り合う元素どうしでもよく似た性質を示す理由は?
■問題
同周期では、原子番号が大きいほど原子半径が小さくなり、同族では原子番号が大きいほど原子半径が大きくなる理由は?
■問題
同一周期の原子のイオン化エネルギーは、原子番号が大きくなるにつれて増加する傾向を示す理由は?
■問題
酸化マグネシウム、酸化カルシウムは塩化ナトリウム、塩化カリウムに比べて融点が高くなる理由は?(イオン間の距離は考えなくてよい。)
■問題
メタン分子が極性をもたず、アンモニア分子が極性もつ理由は?
■問題
金属は電気伝導性や熱伝導性が大きい理由は?
■問題
金属が延性や展性を示す理由は?
■問題
塩化ナトリウムの水溶液が電気伝導性を示す理由は?
■問題
氷から水になるときに、体積が減少する理由は?
■問題
皮膚をアルコールで消毒するとき、冷たく感じる理由は?
■問題
乾いた空気と湿った空気とでは、乾いた空気の方が密度が大きい理由は?
■問題
閉め切った室内で炭を燃やし続けると危険である理由は?
■問題
冬の寒い日、雨でぬれた道路に、塩化カルシウムをまくと凍結しにくい理由は?
■問題
質量モル濃度の等しいグルコース水溶液と塩化ナトリウム水溶液では、塩化ナトリウムの方が沸点が高い理由は?
■問題
ある物質を溶かした希薄溶液では過冷却が見られた後、水平ではなく液温が次第に下がりながら溶液が凝固していく。この理由は?
■問題
不揮発性物質を溶質とする溶液の蒸気圧は、純溶媒の蒸気圧より低くなる理由は?
■問題
野菜を濃い食塩水につけると、野菜がしなびる理由は?
■問題
モル濃度の等しいショ糖水溶液と塩化カルシウム水溶液では、塩化カルシウムの方が浸透圧が高い理由は?
■問題
高分子化合物の分子量の決定には浸透圧法が用いられ、凝固点降下法が用いられない理由は?
■問題
コロイド溶液に光線を当てると、光の通路が輝いて見える理由は?
■問題
2本の電極を設置したU字管にコロイド溶液を入れて、直流電圧をかけるとコロイド粒子は陽極または陰極のどちらかに移動する。この現象の理由は?
■問題
タンパク質やデンプンなどのコロイド溶液に多量の電解質を加えると、コロイド粒子が集まり沈殿する。
この理由は?
■問題
水酸化鉄(Ⅲ)水溶液のコロイド溶液に少量の電解質溶液を加えると、コロイド粒子が集まり沈殿する。この理由は?
■問題
アンモニアの工業的製法では、温度を下げた方が平衡の上では有利であるが、比較的高温で行われる理由は?
■問題
水で濡れているホールピペットとビュレットを使用する場合には、それらをとも洗いする必要がある理由は?
■問題
酢酸ナトリウムの水溶液が弱塩基性を示す理由は?
■問題
酢酸と水酸化ナトリウムの水溶液を用いた中和滴定に関して、指示薬としてフェノールフタレインを用いる理由は?
■問題
アンモニア分子は、配位子となり錯イオンを形成するが、アンモニウムイオンは、錯イオンを形成しない理由は?
■問題
シュウ酸水溶液を硫酸酸性にしたのち、70℃に加熱して過マンガン酸カリウム水溶液を滴下して反応させた。指示薬なしに反応の終点がわかる理由は?
■問題
ヨウ素滴定において、ヨウ素の標準溶液は純水ではなく、ヨウ化カリウム水溶液を用いて調製する理由は?
■問題
ダニエル電池において、負極側の硫酸亜鉛水溶液の濃度を低く、正極側の硫酸銅(Ⅱ)水溶液の濃度を高くしておくと、電流はより長く流れるようになる。この理由は?
■問題
ダニエル電池の正極槽と負極槽を仕切っている素焼き板をガラス板に代えると電池としてはたらかなくなる理由は?
■問題
鉛蓄電池は放電によって、電解液である希硫酸の密度が減少する理由は?
■問題
水を電解するときに少量の硫酸を加えるのはなぜか?
■問題
塩化銅(Ⅱ)水溶液を電気分解すると、陰極の表面に銅が析出したのに対して、塩化ナトリウム水溶液を電気分解すると、陰極の表面にナトリウムは析出しなかった。ナトリウムが析出しない理由は?
一部の問題例ですが
どうでしょうか?
どれだけ、理由を記述できますか?
☆聴いて覚える化学シリーズ
「理由を問う記述問題 無機・有機・理論化学編」
の音声&テキストは
恋する化学より
ご購入いただけます。(データはDVD-Rに入れて発送)
★今すぐ欲しい方は、下記DLマーケットにてご購入いただけます。
↓ランキングが見れます。↓
にほんブログ村
↓ランキングが見れます。↓
にほんブログ村
こうやって覚えよう!グルコールの構造式の書き方!
単糖類であるグルコースは,結晶中で六員環構造をとっています。
その六員環構造には,α-グルコースとβ-グルコースの2種類があります。
今日は,そのα-グルコースとβ-グルコースの構造式の書き方を紹介します。
★グルコースの書き方
1. 六角形を書く。(右上から右回りに①~⑥とする。)
2. ①の位置に原子Oを書く。
3. 縦線を5本書く。
4. ⑥の位置の上にCH2OHを書く。
5. α-グルコースの場合,④の上,②,③,⑤の下にOHを書く。
β-グルコースの場合,②,④の上,③,⑤の下にOHを書く。
α-グルコースとβ-グルコースは,互いに光学異性体の関係にあり,
一位(①)の炭素原子に結合する-OHの位置が上下反対になっていることがポイントです!
☆★☆覚え方☆★☆
β-グルコースは①からOHが上下上下となると覚えて,α-グルコースは①の位置が逆と覚える!
グルコースは水溶液中では,六員環構造のα-グルコースとβ-グルコースと五員環構造(鎖状構造)のアルデヒド型グルコースの3種類が平衡状態となっています。
アルデヒド型グルコースには,アルデヒド基が存在するため,グルコースの水溶液は還元性を示します。
このことは入試でよく問われるのでしっかりおさえましょう!
ここで,多糖類であるデンプンとセルロースの構造についても一緒におさえましょう。
デンプンは,アミロースとアミロペクチンの2つの成分から構成されています。
アミロースとアミロペクチンはともに,多数のα-グルコースが脱水縮合したもので,前者は直鎖状のらせん構造,後者は枝分かれしたらせん構造からなります。
一方,セルロースは,多数のβ-グルコースが脱水縮合した直鎖状の構造からなります。
デンプンの水溶液にヨウ素ヨウ化カリウム水溶液(ヨウ素溶液)を加えると, 青紫色に呈色します。
この反応をヨウ素デンプン反応といい,ヨウ素やデンプンの検出に用いられます。
デンプンが呈色する理由は,α-グルコースが脱水縮合してできたらせん構造の中に,ヨウ素分子I2が入り込むためで,セルロースはらせん構造をもたないために呈色しません。
このことからヨウ素デンプン反応によって,デンプンとセルロースとを判別できます。
拙著
『くらべてつなげてまとめる数学 (数学Ⅰ、A、Ⅱ、Bをネットワークでつなぐ)/文英堂』
¥1、296
Amazon.co.jp
も宜しくお願い致します。
無機化学と有機化学の参考書は、下記DLマーケットにて販売しています。
【「くらべてつなげてまとめる無機化学」 第一部】
【「くらべてつなげてまとめる無機化学」 第二部】
【「くらべてつなげてまとめる有機化学」 第一部】
【「くらべてつなげてまとめる有機化学」 第二部】
↓ランキングが見れます。↓
にほんブログ村
↓ランキングが見れます。↓
にほんブログ村
ん?わけわからん!最も難しいテーマの1つペプチドの構造決定問題!
ペプチドに関する問題は知識問題だけでなくペプチドの配列や構造を決定する問題がよく出題されます。
この構造決定問題を解くには、知識プラス論理的な思考が必要とされ、高校化学で最も難しいテーマの1つです。
おそらく、複雑な構造決定問題は解説を見ても完全に理解できない人も多くいるのではないでしょうか。
「ペプチドの構造決定 完全攻略チャート&過去問題解説集」では、「構造決定のポイント」と「推定手がかり」を大きく5つ、細かく12アイテムに分類し、市販されているどの参考書、問題集よりもわかりやすく丁寧に解説しています。
それでは、その商品の中身を少し紹介・解説したいと思います。
■ペプチドとは?
2個のアミノ酸のうち、一方のアミノ酸のカルボキシ基(-COOH)と他方のアミノ酸のアミノ基(-NH2)から水分子がとれて、縮合してできたアミド結合-CONH-を、特にペプチド結合といいます。
2分子のアミノ酸が縮合してできたペプチドをジぺプチド、3分子のアミノ酸が縮合したものをトリペプチド、10個以上のアミノ酸が縮合重合したものをポリペプチドといいます。
タンパク質の基本構造は、多種のアミノ酸がペプチド結合により結合したポリペプチドをもちます。
■ペプチドの構造決定
ペプチドの構造を決定するためのポイント以下のように大きく5つになります。
この分類は私のオリジナルでどの参考書にも載っていません。
Ⅰ.異性体
例えば、グリシンとアラニンからなるジペプチドの場合は、グリシンの-COOH基とアラニンの-NH2基とが脱水縮合してできたグリシルアラニン(Gly-Ala)のほか、グリシンの-NH2基とアラニンの-COOH基とが脱水縮合してできたアラニルグリシン(Ala-Gly)が存在し、これらは構造異性体の関係にあります。
つまり、Gly-AlaとAla-Glyは、異なるジペプチドとなり、ペプチド結合には、必ず2通りの結合の仕方があります!
さらに、「光学異性体を含めて異性体の数を求めよ。」と言われた場合、アラニンには不斉炭素原子が1個存在するので、2種類ある構造異性体のそれぞれについて、2種(D体、L体という)の光学異性体が存在します。よって、異性体の総数は2×2=4種類となります。
Ⅱ.検出反応
タンパク質(ペプチド)の検出反応は、キサントプロテイン反応、ビウレット反応、硫黄反応の3つが頻出!
フェノール類の検出反応でよく出る塩化鉄(Ⅲ)との反応もたまにでるので、一緒に頭に入れておきましょう。
Ⅲ.分子量
問題文中に、「ペプチドやアミノ酸の分子量」が与えられている場合は、かなり有効な手がかりとなります。
答えだけを求める場合は、適当にアミノ酸を組わせて、分子量を計算してペプチドを求めることもできます。
Ⅳ.ペプチドの特有反応
ペプチドは、酸や塩基や酵素によって、ペプチド結合が切れ、加水分解されます。
例えば、「①-②-③のトリペプチドを加水分解すると、ジペプチドとアミノ酸になった」とあったら、
①-②と③、①と②-③の2通りの可能性があることに注意しましょう。
Ⅴ.等電点・電気泳動
例えば、「アミノ酸AをpHxの緩衝溶液中で電気泳動すると、陽極(陰極)に移動した。」とあったら、
アミノ酸Aは、pH=xで陰イオン(陽イオン)となっている。
さらに→
アミノ酸Aの等電点は、xより小さい(大きい)。
ことがわかります。
以上、簡単に5つのポイントについて解説しました。
「ペプチドの構造決定 完全攻略チャート&過去問題解説集」では、これら5つのポイントをオリジナル「推定アイテム」を12個を用いて具体的に詳しくまとめて解説しています。
特に、医・薬系や難関大学を志望する学生は、この分野が合否を左右するので、騙されたと思って一度目にしてほしいです。
過去問題も8大学と盛りだくさん。
これだけやれば確実にマスターできます。
■収録出題校
奈良県立医科大学(2013)、北海道大学(2013)、北里大学(2013)、同志社大学(2013)、群馬大学(2013)、広島大学(2013)、大阪医科大学(2013)、早稲田大学(2011)
問題のみはココみれます。
商品はHP「恋する化学」からご購入いただけます。
★今すぐpdfデータをほしい方は、下記よりご購入いただけます。
拙著
『くらべてつなげてまとめる数学 (数学Ⅰ、A、Ⅱ、Bをネットワークでつなぐ)/文英堂』
¥1、296
Amazon.co.jp
も宜しくお願い致します。
無機化学と有機化学の参考書は、下記DLマーケットにて販売しています。
【「くらべてつなげてまとめる無機化学」 第一部】
【「くらべてつなげてまとめる無機化学」 第二部】
【「くらべてつなげてまとめる有機化学」 第一部】
【「くらべてつなげてまとめる有機化学」 第二部】
↓ランキングが見れます。↓
にほんブログ村
↓ランキングが見れます。↓
にほんブログ村
医薬系大学志望の人は必須!医薬品に関する問題
医薬品に関する入試問題は、ほぼ知識問題で覚えれば確実に点数を取ることができます。
また、問われるものも他の分野と比較するとそう多くはないので、いかに整理して覚えるかが鍵となります。
医薬品に関する問題 完全攻略チャート&過去問解説集では、大きく対症療法薬・化学療法薬・殺菌・消毒薬の3つに分類し、市販されているどの参考書、問題集よりもわかりやすく丁寧に解説しています。
それでは、その商品の中身を少し紹介・解説したいと思います。
■対症療法薬とは?
「病気を直接治すのではなく症状を緩和するはたらきをする薬」のことをいい、対症療法薬で出題されるのは、ほとんどが解熱鎮痛剤です。(他には消炎鎮痛剤のサリチル酸メチル)この解熱鎮痛剤の代表例であるアセチルサリチル酸とアセトアミノフェンの ①開発の流れ、②合成経路と化合物の構造を覚えることが最大のポイントとなります。
■化学療法薬とは?
「病原体(菌)に直接作用し,死滅させることによって病気を治療する薬」のことをいい、化学療法薬は、「抗生物質(微生物によって生産され、他の微生物の発育や代謝を阻害する物質)=天然抗菌剤」と「合成抗菌剤」のサルファ剤(スルファルアミドの骨格をもつ総称)の2つが頻出となります。
☆ポイントは,次の3つ!
① 抗生物質は,ペニシリンとストレプマイシンの2つを覚える。
② 化合物の構造は、スルファルアミドが書ければよい。
③ ペニシリン、ストレプマイシン、サルファ剤の作用する要因を覚える。
★作用する要因
ペニシリン …… 細菌の細胞壁を合成する酵素の働きを阻害。
ストレプマイシン …… タンパク質を合成する酵素の働きを阻害。
サルファ剤 …… 葉酸を合成する酵素の働きを阻害。
■殺菌・消毒薬とは?
「細菌などの生存や繁殖を阻害して感染を防ぐことを目的とする薬」のことをいい、その効果をあらわすもとになる化学変化によって、大きく2つのグループに分けることができます。
その化学変化の作用とそのグループに含まれる物質を整理して覚えることが最大のポイントとなります。
■その他の覚えておきたい用語
選択毒性 …… 人体の特定の病原菌・癌細胞などに作用して毒性を示し、他の有益な菌や正常細胞には害を与えないこと。
耐性薗 …… 抗生物質などの抗菌剤に対する抵抗性が著しく高くなった細菌。
生薬 …… 天然に存在する薬効を持つ産物から、有効成分を精製することなく用いる薬の総称。
副作用 …… 医薬品に期待される薬理作用とは異なった治療目的に沿わない作用。
プロスタグランジン …… 発熱や痛みの原因物質。
以上、簡単にポイントを解説しました。
医薬品に関する問題 完全攻略チャート&過去問解説集これらのポイントをどの参考書よりもわかりやすくまとめて解説しています。
特に、医・薬系や難関大学を志望する学生は、騙されたと思って一度目にしてほしいです。
過去問題も16大学と盛りだくさん。
これだけやれば確実にマスターできます。
■収録出題校
岐阜大学(2013)、同志社大学(2013)、昭和大学(2013)、信州大学(2013)、大阪医科大学(2013)、富山大学(2012)、東京理科大学(2012)、長崎大学(2012)、大阪市立大学(2012)、広島大学(2012)、岡山大学(2012)、熊本大学(2009 2010)、新潟大学(2011)、立命館(2011)、名城大学(2011)、摂南大学(2009)
問題のみはココみれます。
商品はHP「恋する化学」からご購入いただけます。
★今すぐpdfデータをほしい方は、下記よりご購入いただけます。
拙著
『くらべてつなげてまとめる数学 (数学Ⅰ、A、Ⅱ、Bをネットワークでつなぐ)/文英堂』
¥1、296
Amazon.co.jp
も宜しくお願い致します。
無機化学と有機化学の参考書は、下記DLマーケットにて販売しています。
【「くらべてつなげてまとめる無機化学」 第一部】
【「くらべてつなげてまとめる無機化学」 第二部】
【「くらべてつなげてまとめる有機化学」 第一部】
【「くらべてつなげてまとめる有機化学」 第二部】
↓ランキングが見れます。↓
にほんブログ村
↓ランキングが見れます。↓
にほんブログ村
2次試験まで残りわずか!医歯薬系大学を受ける人は必見!核酸に関する問題
核酸に関する問題は、医歯薬系大学でよく出題されるのですが、学校の授業で習ってなかったり、参考書では詳しく解説されていないため、多くの学生が苦手としています。
しかし、核酸に関する問題は、他の分野と比較すると、覚えることは少ないので整理して理解すれば短時間でマスターすることができます。
核酸に関する問題 完全攻略チャート&過去問解説集出題タイプを8つに分類し、これ以上ないくらいにわかりやすくまとめました。
はっきり断言します!!!!!!
どの参考書よりもわかりやすく短時間でマスターできます!
2次試験まで時間がなくて焦っている受験生は必見です!
それでは、その商品の中身を少し紹介・解説したいと思います。
■核酸とは?
細胞には、糖類、タンパク質、脂質などの他、核酸とよばれる酸性の高分子化合物が存在します。
核酸は、構成成分の糖(五炭糖=ペントース)の種類により、大きく分けて2種類あり、一方はデオキシリボ核酸(DNA:Deoxyrido Nucleic Acid)、もう一方はリボ核酸(RNA:Ribo Nucleic Acid)といいます。
核酸に関する問題は、大きくⅠ~Ⅷの8つの出題タイプがあります。
この8つのタイプを整理して覚えることが最大のポイントです!
Ⅰ.ヌクレオシドとヌクレオチドに関する問題
核酸(DNA、RNA)は、リン酸(H3PO4)、糖(五炭糖)、有機塩基の3つから構成されます。
糖と有機塩基が結合したものをヌクレオシドとよび、それにリン酸が結合したものをヌクレオチドとよびます。
さらに、ヌクレオチドが縮合重合したものは、ポリヌクレオチドとよばれます。
つまり、核酸はヌクレオチドを繰り返し単位とする高分子化合物です。
Ⅱ.DNAとRNAの構成物質の違いに関する問題
核酸(DNA、RNA)は、リン酸、糖、有機塩基の3つから構成されます。
しかし、DNAとRNAでは糖と有機塩基部分がそれぞれ異なります。
この違いが非常によく狙われます!
ⅰ.糖部分
DNAでは、糖はデオキシリボースで、RNAでは、糖はリボースとなります。
ⅱ.有機塩基部分
DNAでは、有機塩基は、アデニン(A)、グアニン(G)、シトシン(C)、チミン(T)の4種類からなり、RNAでは、有機塩基は、アデニン(A)、グアニン(G)、シトシン(C)、ウラシル(U)の4種類からなります。
Ⅲ.核酸の構成元素に関する問題
核酸(DNA、RNA)の構成元素を問う問題は、正誤問題でよく狙われます。
DNA、RNAの構成単位は、リン酸(H3PO4)、糖、有機塩基で、
構成元素はリン酸は、H、P、O、
糖は、C、H、O,
有機塩基は、C、H、N、Oであるので、
DNA、RNAの構成元素は、いずれもC、H、N、O、Pの5元素となります。
Ⅳ.核酸の結合に関する問題
入試では、「ⅰ.リン酸と糖」、「ⅱ.有機塩基と糖」、「ⅲ.DNAの二本鎖」の3つの結合が狙われます。
ⅰ、ⅱでは、糖のどの位置で脱水縮合するのかもおさえましょう。
簡単にまとめると(※チャートでは図を用いて詳しく解説しています。)
リン酸と糖の結合 …… エステル結合(リン酸エステル結合)
有機塩基と糖の結合 …… グリコシド結合
ヌクレオチドどうしの結合 …… エステル結合(リン酸エステル結合)
DNAの二本鎖の結合 …… 水素結合
Ⅴ.核酸,糖,有機塩基の構造に関する問題
ⅰ.糖の構造
糖の構造を問う問題は、ほとんどが選択問題で、書かせることはあまりありません。デオキシリボースは、リボースの2位のヒドロキシ基-OHが-Hに置換された化合物であることをおさえましょう!
ⅱ.有機塩基の構造
有機塩基の構造を問う問題も糖の構造と同様に、ほとんどが選択問題なので、5つの構造式を見て塩基名が何になるかわかればよいです。
ⅲ.DNAとRNAの構造
ヌクレオチドの糖部分とヌクレオチドのリン酸部分とが縮合重合してできた化合物をポリヌクレオチドといいました。
このポリヌクレオチドの高分子鎖が核酸です。
RNAは、この1本の高分子鎖のことをいい、DNAは、2本の高分子鎖が、アデニンとチミン、グアニンとシトシンとの間で水素結合による塩基対をつくり、二重らせん構造を形成しています。
その他
Ⅵ.有機塩基の対となる組み合わせと水素結合の数に関する問題
Ⅶ.DNAの塩基組成に関する問題
Ⅷ.DNAとRNAの所在と役割に関する問題
があります。
以上、簡単にポイントを解説しました。
核酸に関する問題 完全攻略チャート&過去問解説集これらのポイントをどの参考書よりもわかりやすくまとめて解説しています。
特に、医歯薬系や難関大学を志望する学生は、騙されたと思って一度目にしてほしいです。
過去問題も11大学と盛りだくさん。
これだけやれば確実にマスターできます。
■収録出題校
早稲田大学(2013年)、慶應義塾大学(2013年)、日本大学(2013年)、鳥取大学(2012年)、新潟大学(2012年)、明治大学(2012年)、福岡大学(2012年)、早稲田大学(2011年)、北里大学(2011年)、金沢大学(2011年)、香川大学(2011年)、京都薬科大学(2011年)、日本大学(2011年)
問題のみはココみれます。
商品はHP「恋する化学」からご購入いただけます。
★今すぐpdfデータをほしい方は、下記よりご購入いただけます。
拙著
『くらべてつなげてまとめる数学 (数学Ⅰ、A、Ⅱ、Bをネットワークでつなぐ)/文英堂』
¥1、296
Amazon.co.jp
も宜しくお願い致します。
無機化学と有機化学の参考書は、下記DLマーケットにて販売しています。
【「くらべてつなげてまとめる無機化学」 第一部】
【「くらべてつなげてまとめる無機化学」 第二部】
【「くらべてつなげてまとめる有機化学」 第一部】
【「くらべてつなげてまとめる有機化学」 第二部】
↓ランキングが見れます。↓
にほんブログ村
↓ランキングが見れます。↓
にほんブログ村
2次試験まで待ったなし!理由を問う記述問題対策は大丈夫?
今日は、
受験生から好評をいただいている
「☆聴いて覚える化学シリーズ 「理由を問う記述問題 無機・有機・理論化学編」
を再度紹介します。
大学入試の化学の2次試験では、「理由を問う記述問題」がよく出題され合否を大きく左右します。
しかし、どんな理由がよく問われるのか、どのように記述すればいいのか、わかっていない人がほとんどです。
そこで!
国公私立大学の7年分の「理由を問う記述問題」を3年の月日をかけて徹底的に分析し、頻出・覚えておきたい問題を厳選してまとめました。
今日は問題のみを公開したので、是非、チェックしてみてください。
★無機化学編
■□■□■1族・2族元素■□■□■
■問題
リチウムと同じアルカリ金属であるカリウムが、リチウムより激しく水と反応する理由は?
■問題
アルカリ金属の単体は、原子番号が大きいほど融点が低くなる理由は?
■問題
水酸化ナトリウムの固体の質量をはかりとっても、正確な濃度の水溶液を調製することができない理由は?
■問題
アルカリ金属の単体のリチウム、ナトリウム、カリウムを石油中に保存する理由は?
■問題
2族元素の原子が、いずれも2価の陽イオンになりやすい理由は?
■問題
石灰水に二酸化炭素を通すと、白濁する理由は?
■問題
アルカリ土類金属の原子半径は、同周期のアルカリ金属の原子半径と比較すると小さい理由は?
■問題
金属カルシウムの融点は、同周期の1族の金属カリウムの融点に比べて極めて高い理由は?
■問題
実験室で二酸化炭素を発生させる時、石灰石に希塩酸を反応させる。このとき、希塩酸の代わりに希硫酸を用いると、気体の発生が途中で停止してしまう理由は?
■問題
酸化カルシウムが缶入りの酒や駅弁を温める発熱剤として利用される理由は?
■問題
硫酸バリウムが、X線撮影の造影剤に使われる理由は?
■問題
カルシウムの単体をつくるために、カルシウム塩の水溶液を電気分解することが不適当な理由は?
■□■□■14族・15族元素■□■□■
■問題
ドライアイスは、1気圧のもとでは液体にならずに-79℃で昇華する理由は?
■問題
シリカゲルが乾燥剤や吸着剤に使われる理由は?
■問題
ダイヤモンドは電気を通さないが、黒鉛は電気を通す理由は?
■問題
ダイヤモンドは非常に硬いが、黒鉛はもろい(軟らかい)理由は?
■問題
二酸化炭素が水に溶けると酸性を示す理由は?
■問題
二酸化ケイ素の固体は、水に溶けにくい理由は?
■問題
リンの同素体である黄リンを水中で保存する理由は?
■問題
一酸化窒素は水上置換で、二酸化窒素は下方置換で捕集する理由は?
■問題
アンモニアは、実験室では塩化アンモニウムと水酸化カルシウムの混合物を加熱することで得られる。この製法において、
■問題2
アンモニアは、上方置換によって捕集する理由は?
■問題3
アンモニアの乾燥には濃硫酸は不適当である理由は?
■問題
濃硝酸を褐色ビンにいれて冷暗所で保存する理由は?
■問題
窒素は、常温・常圧で化学的に非常に安定である理由は?
■□■□■16族・17族・18元素■□■□■
■問題
水は16族元素の水素化物の中で異常に高い沸点を示す理由は?
■問題
濃硫酸は酸としての性質はきわめて弱く、希硫酸が強酸性を示す理由は?
■問題
希硫酸を調製する場合、必ず水をかき混ぜながら濃硫酸を少しずつ加えなければいけない理由は?
■問題
水は極性分子であり、二酸化炭素は無極性分子である理由は?
■問題
硫化水素は、水に溶けて弱い酸性を示す理由は?
■問題
二酸化硫黄は、水に溶けて弱い酸性を示す理由は?
■問題
ハロゲンの単体は、原子番号が大きいほど融点・沸点が高くなる理由は?
■問題
ハロゲンの単体のうち、フッ素が最も酸化力が強い理由は?
■問題
フッ化水素が他のハロゲン化水素と比較して沸点が著しく高い理由は?
■問題
単体の塩素は酸化マンガン(Ⅳ)に濃塩酸を加えて加熱し、発生する気体を水の入った洗気びんに通して、次に濃硫酸の入った洗気びんに通して捕集します。水と濃硫酸を用いる理由は?
■問題
フッ化水素の水溶液は、ガラス瓶に保存できない理由は?
■問題
次亜塩素酸ナトリウムを含む漂白剤と酸性の洗剤を混ぜると危険な理由は?
■問題
18族元素は、反応性が低く化合物をつくりにくい理由は?
■□■□■金属元素Fe、Al、Ag、Cu、他■□■□■
■問題
水酸化鉄(Ⅱ)の沈殿を含む水溶液をそのまま放置すると、沈殿の色が次第に変化して赤褐色になる。この理由は?
■問題
鉄やアルミニウムの単体は塩酸や希硫酸には溶けるが、濃硝酸や熱濃硫酸にはほとんど溶けない理由は?
■問題
鉄を亜鉛でめっきしたものは、鉄をスズでめっきしたものよりさびにくい理由は?
■問題
ブリキ、トタンの表面に傷がついて鉄が露出したとき、ブリキよりもトタンのほうがさびにくい理由は?
■問題
アルミニウムはイオン化傾向が大きいのにもかかわらず、さびが進行しない理由は?
■問題)
アルミニウムの合金であるジュラルミンが航空機材料などに用いられる理由は?
■問題
アルミニウムイオンを含む水溶液の電気分解では、アルミニウムの単体を得ることができない理由は?
■問題
アルミニウムの融解塩電解の際に氷晶石を加える理由は?
■問題
塩化銀にアンモニア水を加えると溶解する理由は?
■問題
塩化銀を褐色瓶中に保存する理由は?
■問題
銀や銅が塩酸や希硫酸に溶けない理由は?
■問題
硫酸銅(Ⅱ)無水物が水分の検出に用いられる理由は?
■問題
金属イオンの系統分析において、
アルミニウムイオン、カルシウムイオン、銅(Ⅱ)イオン、鉄(Ⅲ)イオン、亜鉛イオンの金属イオンを含む水溶液について、次の操作を順に行った。
操作1 水溶液に塩酸を加えた。その際、沈殿は生じなかった。
操作2 操作1の水溶液に硫化水素を通じると黒色の沈殿が生じたため、ろ過して沈殿Aとろ液に分離した。
操作3 操作2で得られたろ液を煮沸した。次に、硝酸を加え、さらにアンモニア水を過剰に加えると沈殿が生じたため、ろ過して沈殿Bとろ液に分離した。
~以下略~
■問題1
操作3で、ろ液を煮沸する理由は?
■問題2
操作3で、硝酸を加える理由は?
■問題
鉛は硝酸には溶けるが、塩酸や希硫酸には溶けない理由は?
■問題
硫化水素は、湿らせた酢酸鉛紙を黒変する理由は?
★有機化学編
■□■□■炭化水素■□■□■
■問題
アルカン、アルケン、アルキンが水にほとんど溶けない理由は?
■問題
直鎖状のアルカンの沸点は、炭素数が増大するにつれて高くなる理由は?
■問題
エタンは正四面体が2つつながった立体構造であるのに対し、エチレンが平面構造をとる理由は?
■問題
アセチレンに水が付加して生じるビニルアルコールが、すぐにアセトアルデヒドに異性化する理由は?
■□■□■酸素を含む有機化合物■□■□■
■問題
アルコールの水溶液が中性である理由は?
■問題
メタノール、エタノールが水によく溶ける理由は?
■問題
アルデヒドが銀鏡反応を示す理由は?
■問題
エーテルの沸点が、異性体の関係にあるアルコールに比べてかなり低くなる理由は?
■問題
エステルが水に溶けにくい理由は?
■問題
一般に、カルボン酸は酸化されにくいため還元性をもたないが、ギ酸は還元性をもつ理由は?
■問題
酢酸の水溶液は弱酸性を示すが、無水酢酸の水溶液は中性を示す理由は?
■問題
フマル酸は、マレイン酸より融点が高くなる理由は?
■問題
マレイン酸は加熱すると、分子内脱水して無水マレイン酸が生成する。しかし、フマル酸を加熱しても分子内脱水されない理由は?
■問題
油脂が水に溶けない理由は?
■問題
セッケンを水に溶かしたとき、塩基性を示す理由は?
■問題
硬水中で、セッケンの洗浄力が低下する理由は?
■問題
合成洗剤は、硬水中で洗浄力が低下しない理由は?
■問題
油をセッケン水に入れて振ると乳濁液になる理由は?
■問題
セッケンに洗浄作用がある理由を2つ挙げよ。
■問題
セッケンは、絹や羊毛の洗浄には適さない理由は?
■問題
有機化合物を完全に燃焼させて元素分析を行う際に、燃焼によって生成した混合気体を、はじめに塩化カルシウム管に通し、次にソーダ石灰管に通して吸収させる。このとき混合気体を通す順序を逆にしてはいけない理由は?
■□■□■芳香族化合物■□■□■
■問題
ベンゼンを空気中で点火すると、多量のススが出る理由は?
■問題
エチレンの二重結合は付加反応を起こしやすく、ベンゼンの二重結合では、置換反応の方が起こりやすい理由は?
■問題
フェノール類が水に溶けにくい理由は?
■問題
サリチル酸メチル、アセチルサリチル酸のそれぞれに塩化鉄(Ⅲ)水溶液を加えると、サリチル酸メチルだけが呈色した。その理由は?
■問題
安息香酸とフェノールを混合したエーテル溶液に、炭酸水素ナトリウム水溶液を加えてよく撹拌した。静置後、水層とエーテル層に分離したところ、エーテル層にはフェノールのみが含まれていた。この理由は?
■問題
アニリンが塩酸に溶ける理由は?
■問題
アニリンに酢酸を加えて加熱したり、無水酢酸を加えると塩基性を失う理由は?
■問題
アニリンを希塩酸に溶かし、氷で冷却しながら亜硝酸ナトリウム水溶液と反応させるとジアゾ化が起こり、塩化ベンゼンジアゾニウムが生じる。
この反応では、5℃以下に氷冷しながら行う必要がある理由は?
■□■□■天然高分子化合物■□■□■
■問題
単糖類や二糖類が水によく溶ける理由は?
■問題
セルロースが水に溶けにくい理由は?
■問題
グルコースの水溶液が還元性を示す理由は?
■問題
スクロースが還元性を示さない理由は?
■問題
デンプンおよびセルロースに、ヨウ素ヨウ化カリウム水溶液を加えた。デンプンは青~青紫色に呈色したが、セルロースは呈色しなかった。その理由は?
■問題
紙(セルロース)に濃硫酸をたらすと真っ黒くなる理由は?
■問題
木綿や麻が吸湿性に優れている理由は?
■問題
木綿や麻が塩基には比較的強く、酸には弱い理由は?
■問題
グリシンには光学異性体が存在しない理由は?
■問題
アミノ酸が水によく溶ける理由は?
■問題
アミノ酸が他の有機化合物に比べて、融点が高い理由は?
■問題
トリペプチドを溶かした水溶液に、水酸化ナトリウム水溶液を加えた後、硫酸銅(Ⅱ)水溶液を少量加えると赤紫色になった。この呈色はジペプチドでは生じない理由は?
■問題
等電点が9.7のリシンを中性の緩衝溶液に溶解し直流電圧をかけると、陰極側に移動する理由は?
■問題
酵素が加熱により、触媒としての機能を失う理由は?
■問題
タンパク質を加熱したり、酸や塩基を加えると凝固する理由は?
■□■□■合成高分子化合物■□■□■
■問題
ポリビニルアルコールは、その構造式から見るとビニルアルコールの重合により得られると予測される。しかし実際は、ポリ酢酸ビニルの加水分解により合成されている。その理由は?
■問題
ポリビニルアルコールが水溶性である理由は?
■問題
ポリ塩化ビニルの焼却には注意が必要な理由は?
■問題
高分子化合物の融点は、低分子化合物とは異なり、一般に一定の融点を示さない理由は?
■問題
尿素樹脂やメラミン樹脂を加熱すると硬くなる理由は?
■問題
生ゴム(天然ゴム)の大部分は、トランス形ではなく、シス形のポリイソプレンからなる理由は?
■問題
生ゴム(天然ゴム)の弾性は、空気中に長く放置すると失われる理由は?
■問題
生ゴム(天然ゴム)に5~8%の硫黄を加えて、加熱することで弾性が増す理由は?
★理論化学編
■問題
元素を原子番号の小さい順に並べると、20番目までは性質のよく似た元素が周期的に現れる理由は?
■問題
遷移元素では、族としての類似性のほかに同一周期で隣り合う元素どうしでもよく似た性質を示す理由は?
■問題
周期表において、18Arと19Kや27Coと28Niは原子量の順に並んでいない理由は?
■問題
同周期では、原子番号が大きいほど原子半径が小さくなり、同族では原子番号が大きいほど原子半径が大きくなる理由は?
■問題
同一周期の原子のイオン化エネルギーは、原子番号が大きくなるにつれて増加する傾向を示す理由は?
■問題
酸化マグネシウム、酸化カルシウムは塩化ナトリウム、塩化カリウムに比べて融点が高くなる理由は?
(イオン間の距離は考えなくてよい。)
■問題
メタン分子が極性をもたず、アンモニア分子が極性もつ理由は?
■問題
金属に光沢がある理由は?
■問題
金属は電気伝導性や熱伝導性が大きい理由は?
■問題
金属が延性や展性を示す理由は?
■問題
塩化ナトリウムの水溶液が電気伝導性を示す理由は?
■問題
氷から水になるとき、体積が減少する理由は?
■問題
皮膚をアルコールで消毒するとき、冷たく感じる理由は?
■問題
乾いた空気と湿った空気とでは、乾いた空気の方が密度が大きい理由は?
■問題
閉め切った室内で炭を燃やし続けると危険である理由は?
■問題
瓶に入った炭酸飲料の栓を抜いて室温に放置すると、次第に発泡が弱くなる理由は?
■問題
体積一定の気体の圧力は、温度を上げると高くなる理由は?
■問題
実在気体が、温度の上昇にともなって理想気体に近づく理由は?
■問題
冬の寒い日、雨でぬれた道路に、塩化カルシウムをまくと凍結しにくい理由は?
■問題
質量モル濃度の等しいグルコース水溶液と塩化ナトリウム水溶液では、塩化ナトリウムの方が沸点が高い理由は?
■問題
ある物質を溶かした希薄溶液では過冷却が見られた後、水平ではなく液温が次第に下がりながら溶液が凝固していく。この理由は?
■問題
不揮発性物質を溶質とする溶液の蒸気圧は、純溶媒の蒸気圧より低くなる理由は?
■問題
野菜を濃い食塩水につけると、野菜がしなびる理由は?
■問題
モル濃度の等しいショ糖水溶液と塩化カルシウム水溶液では、塩化カルシウムの方が浸透圧が高い理由は?
■問題
高分子化合物の分子量の決定には浸透圧法が用いられ、凝固点降下法が用いられない理由は?
■問題
コロイド溶液に光線を当てると、光の通路が輝いて見える理由は?
■問題
コロイド溶液を限外顕微鏡で観察すると、光った粒子が不規則に動いているのが見える理由は?
■問題
2本の電極を設置したU字管にコロイド溶液を入れて、直流電圧をかけるとコロイド粒子は陽極または陰極のどちらかに移動する。この現象の理由は?
■問題
タンパク質やデンプンなどのコロイド溶液に多量の電解質を加えると、コロイド粒子が集まり沈殿する。
この理由は?
■問題
水酸化鉄(Ⅲ)水溶液のコロイド溶液に少量の電解質溶液を加えると、コロイド粒子が集まり沈殿する。この理由は?
■問題
一般に、濃度を高くする(気体の圧力を上げる)ほど反応速度が速くなる理由は?
■問題
一般に、温度が高くなるほど反応速度が速くなる理由は?
■問題
化学反応において、触媒を加えることによって反応速度が速くなる理由は?
■問題
アンモニアの工業的製法では、温度を下げた方が平衡の上では有利であるが、比較的高温で行われる理由は?
■問題
水で濡れているホールピペットとビュレットを使用する場合には、それらをとも洗いする必要がある理由は?
■問題
ビュレットを高温乾燥器に入れて乾燥させてはいけない理由は?
■問題
酢酸ナトリウムの水溶液が弱塩基性を示す理由は?
■問題
酢酸と水酸化ナトリウムの水溶液を用いた中和滴定に関して、指示薬としてフェノールフタレインを用いる理由は?
■問題
アンモニア分子は、配位子となり錯イオンを形成するが、アンモニウムイオンは、錯イオンを形成しない理由は?
■問題
シュウ酸水溶液を硫酸酸性にしたのち、70℃に加熱して過マンガン酸カリウム水溶液を滴下して反応させた。指示薬なしに反応の終点がわかる理由は?
■問題
ヨウ素滴定において、ヨウ素の標準溶液は純水ではなく、ヨウ化カリウム水溶液を用いて調製する理由は?
■問題
ダニエル電池において、負極側の硫酸亜鉛水溶液の濃度を低く、正極側の硫酸銅(Ⅱ)水溶液の濃度を高くしておくと、電流はより長く流れるようになる。この理由は?
■問題
ダニエル電池の正極槽と負極槽を仕切っている素焼き板をガラス板に代えると電池としてはたらかなくなる理由は?
■問題
鉛蓄電池は放電によって、電解液である希硫酸の密度が減少する理由は?
■問題
水を電解するときに少量の硫酸を加えるのはなぜか?
■問題
塩化銅(Ⅱ)水溶液を電気分解すると、陰極の表面に銅が析出したのに対して、塩化ナトリウム水溶液を電気分解すると、陰極の表面にナトリウムは析出しなかった。ナトリウムが析出しない理由は?
商品はHP「恋する化学」からご購入いただけます。
★今すぐ、解答のpdfデータをほしい方は、下記よりご購入いただけます。
拙著
『くらべてつなげてまとめる数学 (数学Ⅰ、A、Ⅱ、Bをネットワークでつなぐ)/文英堂』
¥1、296
Amazon.co.jp
も宜しくお願い致します。
無機化学と有機化学の参考書は、下記DLマーケットにて販売しています。
【「くらべてつなげてまとめる無機化学」 第一部】
【「くらべてつなげてまとめる無機化学」 第二部】
【「くらべてつなげてまとめる有機化学」 第一部】
【「くらべてつなげてまとめる有機化学」 第二部】
↓ランキングが見れます。↓
にほんブログ村
↓ランキングが見れます。↓
にほんブログ村
絶対に損はさせません!壁orノートに貼って覚えるポイント・まとめ集
受験生からもっと早くほしかった!との声が多数届いたので、
再度お知らせさせていただきます!
『壁orノートに貼って覚えるポイント・まとめ集』の無機化学編と有機化学編の紹介です。
■特徴1
全国の国公立私大の入試問題(過去7年分)が入力されたデータベースソフトを用いて,徹底的に入試に出るポイントを分析。
■特徴2
他の参考書には載っていない,見たことのないようなポイントやまとめ表を掲載。
例えば……
□X線の遮蔽剤といえば?
X線の造影剤と言えば?
マニアックな知識ではなく,これらは意外と入試で出題されています!
こんな形で掲載
↓ ↓ ↓ ↓
□硫化カドミウムCdS,クロム酸鉛(Ⅱ)PbCrO4,酸化亜鉛ZnO,硫酸バリウムBaSO4,酸化鉄(Ⅲ)Fe2O3
これらに共通する用途は?
こんな形で掲載
↓ ↓ ↓ ↓
□ケイ素Si,リンP,硫黄Sの単体にうち天然に存在するものは?
こんな形で掲載
↓ ↓ ↓ ↓
□水酸化ナトリウムNaOH,水酸化カリウムKOH,リン酸H3PO4,塩化カルシウムCaCl2,塩化マグネシウムMgCl2,塩化鉄(Ⅲ)六水和物
これらの物質に共通する性質は?
こんな形で掲載
↓ ↓ ↓ ↓
□6つの主要なアセトンの製法を言えますか?
こんな形で掲載
↓ ↓ ↓ ↓
□2つの主要な乾留の反応を言えますか?
こんな形で掲載
↓ ↓ ↓ ↓
■特徴3
くらべてつなげてまとめる表を多数掲載
人間の脳は、事柄と事柄をシナプスで繋ぎ、記憶していくことから、英単語などを記憶する際には、グループごとに分類したり、関連するイメージでつなげて覚えていくと、効率的に語彙を増やし、忘れにくいことなどが知られています。
そこで,くらべてつなげて覚えられるようにまとめました。
例えば……
こんな形で掲載
↓ ↓ ↓ ↓
■特徴4
豊富な色を使用。
化学は,呈色反応や化合物などの色を問う問題がよく出題されることから,色がついた文字色を何度も見ることによって記憶がより定着します。
例えば……
□白煙が生じる2つの反応を挙げられますか?
こんな形で掲載
↓ ↓ ↓ ↓
□銅と銀の主要な化合物の色を言えますか?
こんな形で掲載
↓ ↓ ↓ ↓
□典型・遷移金属の主要な酸化物の色を言えますか?
こんな形で掲載
↓ ↓ ↓ ↓
□主要な水和物の色を言えますか?
こんな形で掲載
↓ ↓ ↓ ↓
■特徴5
「キーワード連想」を掲載
当然ながら、入試は時間が勝負です。
そこで,あるキーワードがでたら,ポイントがすぐに連想できるようになるようにまとめました。
例えば…
□天然ガスから分離 or 沸点が最も低い or イオン化エネルギーが最も大きい or 最も理想気体に近い気体とあったら?
□空気中で最も多く存在する希ガスとあったら?
□白色顔料,医薬品,化粧品とあったら?
□黒い多量のススとあったら?
□果実の成熟作用,植物ホルモンとあったら?
□強い光を放って燃焼とあったら?
こんな形で掲載
↓ ↓ ↓ ↓
★他にも掲載している例を紹介します。
□リン酸カルシウムからリン酸までの反応の流れが言えますか?
こんな形で掲載
↓ ↓ ↓ ↓
□二酸化ケイ素からシリカゲルまでの反応の流れが言えますか?
こんな形で掲載
↓ ↓ ↓ ↓
□次の酸のうち揮発性の酸はどれですか?
硝酸,塩酸,フッ化水素酸, 酢酸,濃硫酸
こんな形で掲載
↓ ↓ ↓ ↓
□希硫酸と濃硫酸の性質を言えますか?
こんな形で掲載
↓ ↓ ↓ ↓
□無機化学において,水素が発生する頻出の反応を何個挙げられますか?
こんな形で掲載
↓ ↓ ↓ ↓
□次のアルミニウムに関する用語を説明できますか?
ボーキサイト,アルマイト,アルミナ,ジュラルミン,テルミット
こんな形で掲載
↓ ↓ ↓ ↓
□混同しやすい無水物の生成反応
こんな形で掲載
↓ ↓ ↓ ↓
□有機化合物のにおい
こんな形で掲載
↓ ↓ ↓ ↓
□ナトリウムフェノキシドの2つの生成反応
こんな形で掲載
↓ ↓ ↓ ↓
□有機化合物で登場する水酸化ナトリウムNaOHの反応
こんな形で掲載
↓ ↓ ↓ ↓
□混同しやすい有機化合物の反応
こんな形で掲載
↓ ↓ ↓ ↓
□こんな図表とか
↓ ↓ ↓ ↓
これらはほんの一部です!
この『壁orノートに貼って覚えるポイント・まとめ集』を壁やノートに貼って毎日眺めることで暗記が大幅に短縮できます!
pdfデータ形式になっているので,何枚でもプリントでき,いろんなところに貼ったり,携帯することができます。
絶対にお得です!
下記は,有機化学編の表紙(A4サイズ)です。
下記は,無機化学編のサンプル(A4サイズ)です。
下記,DLマーケットよりご購入いただけます。
【壁orノートに貼って覚えるポイント・まとめ集 有機化学編】
pdfデータ(A4サイズ 12枚) 価格 1,000円
【壁orノートに貼って覚えるポイント・まとめ集 無機化学編】
pdfデータ(A4サイズ 17枚) 価格 1,000円
人工知能対世界最強棋士の囲碁対決の衝撃!
人工知能(グーグルの研究グループが開発したコンピューターソフト「アルファ碁」)対世界最強棋士の囲碁対決。
4戦目で人間が初勝利!
私は囲碁のプロ棋士を目指していたこともあり、この対決は非常に注目していた。
(ちょっと自慢だが、中学、高校と全国大会に3度出場し、高校時1年時に団体戦で全国5位になったことがある。団体戦の個人では全勝した。)
正直、対戦前は圧倒的にプロが勝つと予想していた。
なぜなら、これまでのコンピューターの実力はプロ棋士には遠く及ばないレベルで、囲碁の対局パターンは10の360乗以上にもなり、コンピューターが人間に勝つにはあと10年くらいはかかると言われてきたからだ。
しかし、蓋を開けると、なんとアルファ碁の3連勝。
衝撃的な強さで度肝を抜かれた。
いつの間に…
としばらくショック状態だった。
恐るべし、グーグル!!!!
しかし、コンピューターにも弱点があることが少しずつわかってきた。
それは囲碁のルールがわからない人には通じないが、
「コウ」
に弱いことだ。
コウを極力避ける傾向にある。
また、ほんのごくたまに乱れることもある。
しかし、これもすぐに克服してくるだろう。
今後、人間はコンピューターには敵わないとなると囲碁界はどうなって行くのだろうか……
いや囲碁界だけではない。
いずれ人間がコンピューターに支配される日がやってくるのかもしれない。